Zločiny spoločnosti Pfizer proti našim deťom: zástava srdca dvojmesačného dieťaťa hodinu po experimentálnej vakcíne
58 detí, ktoré dostali mRNA vakcíny COVID-19, malo život ohrozujúce nežiaduce udalosti
Analýza správ VAERS ukazuje, že na rozdiel od informačného dokumentu FDA, ktorý tvrdí, že väčšina nežiaducich udalostí v klinickom skúšaní spoločnosti Pfizers nebola vážna – najmenej 58 prípadov život ohrozujúcich vedľajších účinkov u dojčiat mladších ako 3 roky, ktoré dostali vakcíny mRNA. boli nahlásené. U niektorých nie je jasné, či prežili. Nie je tiež jasné, prečo boli dojčatá očkované a či boli súčasťou klinických skúšok. Na nadchádzajúcom stretnutí FDA v stredu však FDA nebude môcť tvrdiť, že nevedel
"Bolesť v hrudi; zástava srdca; Studená vlhká pokožka“. Tento krátky popis zástavy srdca, ku ktorej došlo hodinu po podaní vakcíny Pfizer-BioNtech COVID-19, je prevzatý zo systému VAERS – US Vaccine Adverse Eve Reporting System ( číslo prípadu 1015467 ) a netýka sa staršiemu človeku, ani mladému dospelému či dokonca tínedžerovi. Je ťažké uveriť, ale táto správa sa týka dvojmesačného dieťaťa .
„2-mesačný mužský pacient dostal bnt162b2 (PFIZER-BioNtech VACCINE COVID-19) číslo šarže: EL 739 prostredníctvom nešpecifikovaného spôsobu podania dňa 2. februára 2021 v jednej dávke na imunizáciu COVID-19“, tak je uvedené v správa. „Pacient, ktorému bolo podané očkovanie, pozorovaný 15 minút, opustil kliniku a potom sa vrátil o hodinu neskôr 2. februára 2021, prejavoval sa ako studená koža, vlhká a s bolesťou na hrudníku, potom sa rozvinula zástava srdca, pacient stabilizovaný a prevezený na ďalšie lekárske ošetrenie... Výsledok z udalostí nebolo známe. Tento prípad bol hlásený ako závažný s kritériom závažnosti – život ohrozujúci HA. Nie sú možné žiadne následné pokusy. Nečakajú sa žiadne ďalšie informácie."
Ako dostalo 2-mesačné dieťa vakcínu mRNA? Tieto vakcíny zatiaľ nezískali EUA (Emergency Use Authorization) na použitie u detí vo veku päť a menej zo strany FDA alebo akéhokoľvek iného regulačného úradu, a aj keby to tak bolo, EUA bude zahŕňať iba deti vo veku 6 mesiacov a staršie.
Bolo toto dieťa účastníkom klinických skúšok spoločnosti Pfizer-BioNTech, ktoré testovali účinnosť a bezpečnosť medzi deťmi?
Odpoveď je nejasná. Podľa osoby, ktorá napísala správu „Nie som si istý, či bol pacient zaradený do klinického skúšania“. Autor správy však tiež uvádza, že správu „ prijala od kontaktovateľného iného zdravotníckeho pracovníka spoločnosť Pfizer z Regulačnej agentúry“ . Táto poznámka naznačuje, že dieťa sa mohlo skutočne zúčastniť súdneho konania spoločnosti Pfizer. Správa regulačnej agentúry Safety Report Unique Identifier GB-MHRA-ADR 24687611 – uvádza, že správa pochádza z Veľkej Británie (prvé 2 písmená v ID správy predstavujú krajinu pôvodu, GB-Veľkú Britániu a MHRA označujú, že zdroj hlásenia bola jeho „drogová autorita).
Prečo nesledovali stav 2-mesačného dieťaťa po tom, čo hodinu po podaní experimentálnej vakcíny došlo k zástave srdca? Prečo neexistujú žiadne ďalšie informácie? Je to preto, že zomrel? Alebo bolo dieťa odstránené z experimentu? Prečo by to autor správy nespomenul?
Šokujúco sa ukazuje, že tento incident nie je izolovaný, ale v skutočnosti je jedným z mnohých v systéme VAERS, ktorý popisuje bábätká a deti mladšie ako päť rokov vystavené vakcínam mRNA Covid, ktoré utrpeli život ohrozujúce nežiaduce reakcie.
Aj keď deti mladšie ako päť rokov neboli považované za vhodné na tieto vakcíny, pokiaľ neboli súčasťou klinickej štúdie, prekvapivo sa zdá, že v systéme je veľa správ, ktoré opisujú očkované bábätká a batoľatá. Niektoré z detí trpeli život ohrozujúcimi nežiaducimi udalosťami. V niektorých prípadoch nie je jasné, čo sa s nimi stalo; či prežili a uzdravili sa, či ešte stále trpia zdravotnými problémami, alebo zomreli.
O pár dní, 15. júna, bude Poradný výbor pre vakcíny a príbuzné biologické produkty FDA diskutovať o žiadostiach spoločnosti Moderna a Pfizer o EUA vakcíny pre dojčatá a batoľatá vo veku od 6 mesiacov do 4 rokov – jedinú skupinu, ktorá ešte nemá nárok na očkovanie proti COVID-19. dnes.
Podľa brífingového dokumentu FDA zverejneného dnes pred zasadnutím výborov VRBPA bolo do systému VAERS „245 správ z USA“ „u detí vo veku od 6 mesiacov do 4 rokov“, ktoré boli injekčne podané („produkt podaný pacientovi nevhodného vek“ alebo „použitie mimo označenia“) alebo vystavené očkovacej látke „prostredníctvom materského mlieka“. Obe spoločnosti však už v máji oznámili, že ich zistenia naznačujú, že ich vakcíny sú bezpečné a účinné.
V BRBPAC Briefing Document sú uvedené rôzne nežiaduce udalosti hlásené po vystavení vakcíne v tejto vekovej skupine, vrátane „pyrexie..., telesnej teploty..., kašľa, bolesti hlavy, vyrážky, hnačky“ . Podľa dokumentu „Medzi americkými hláseniami VAERS pre jednotlivcov vo veku od 6 mesiacov do 4 rokov, ktoré môžu odrážať neoprávnené použitie očkovacej látky alebo môžu odrážať chybu v hlásení, väčšina (96,3 %) nebola vážna“.
Zatiaľ čo dokument špecifikuje bezpečnostné obavy identifikované z údajov z postregistračného dohľadu nad bezpečnosťou v VAERS, vrátane anafylaxie, myokarditídy a perikarditídy, nesúvisí s týmito bezpečnostnými problémami identifikovanými v mladšej vekovej skupine. Namiesto toho uvádza: „Nebola identifikovaná žiadna nezvyčajná frekvencia, zhluky alebo iné trendy nežiaducich udalostí, ktoré by naznačovali nové bezpečnostné obavy“.
Ale je to naozaj tak? Zdá sa, že bez ohľadu na výsledky a napriek znepokojivým a šokujúcim zisteniam, ktoré vychádzajú z dokumentov spoločnosti Pfizer, sa očakáva, že obe spoločnosti veľmi skoro získajú požadované emisné kvóty. V skutočnosti webová stránka CDC už v apríli propagovala protokol týkajúci sa očkovania detí , ktorý zahŕňal aj deti vo veku od 6 mesiacov do 4 rokov.
Vo svetle tohto očakávaného schválenia RT Magazine vykonal analýzu prípadov hlásených v systéme VAERS, ktoré sa týkali detí do 3 rokov.
Počas analýzy boli odstránené prípady, v ktorých sa uvádzalo, že k expozícii vakcíne došlo prostredníctvom dojčenia (tieto prípady boli analyzované samostatne a čoskoro budú prezentované v nasledujúcom článku), ako aj prípady, ktoré boli identifikované ako chyby v registráciu veku.
Analýza ukazuje, že u dojčiat a batoliat vo veku 3 rokov a mladších bolo najmenej 58 prípadov závažných a život ohrozujúcich nežiaducich reakcií. Toto zistenie je obzvlášť záhadné vzhľadom na skutočnosť, že v tomto veku nemali byť očkované. Žiaľ, podobne ako v prípade uvedenom vyššie, väčšina správ VAERS neuvádza, ako a za akých okolností boli vystavení vakcíne – boli účastníkmi skúšok spoločností? A ak nie, prečo a za akých okolností boli očkované?
Obe spoločnosti zatiaľ nezverejnili bezpečnostné údaje zo svojich skúšok v tejto vekovej skupine. Jedna vec je však jasná zo správ VAERS: bolo veľa detí, ktoré boli zranené po podaní vakcíny. Bez ohľadu na to, či boli očkovaní v testoch alebo nelegálne vo svojich komunitách, spoločnosti Pfizer a Moderna rozhodne nebudú môcť pri predkladaní svojich údajov FDA tvrdiť, že vakcína je pre deti bezpečná. a že v tejto vekovej skupine sa nevyskytli žiadne závažné nežiaduce udalosti. Navyše, experti výboru FDA, ktorí budú diskutovať o schválení EUA, nebudú môcť ignorovať tieto prípady a argumentovať, že nevedeli. Údaje prezentované v tomto článku bez akýchkoľvek pochybností preukazujú úplný opak a tentoraz – tieto údaje sú verejnosti prezentované vopred, pred udelením EUA a pred diskusiou VRBPAC.
Výsledok udalostí: Nezotavilo sa
Jedna z najmrazivejších správ sa týka 43-dňovej ženy, ktorá 30. januára 2021 dostala vakcínu Comirnaty od spoločnosti Pfizer. V popise incidentu (správa č. 1133837) je jasne uvedené, že bola očkovaná a že vakcína bola podaná do svalu: „43-dňová pacientka dostala bnt162b2 (COMIRNATY), intramuskulárne dňa 30. januára 2021 (číslo šarže: EK9788) ako JEDNA DÁVKA na imunizáciu COVID-19“ . Bábätko hneď po očkovaní utrpelo rôzne život ohrozujúce multisystémové poranenia, ako napr „Anafylaktická reakcia (široká), astma/bronchospazmus (úzky), anticholinergný syndróm (široký), akútna centrálna respiračná depresia (široká), pľúcna hypertenzia (široká), kardiomyopatia (široká), eozinofilná pneumónia (široká), vestibulárne poruchy (široká) , Precitlivenosť (široká), Respiračné zlyhanie (úzke), Reakcia na liek s eozinofíliou a syndróm systémových symptómov (široký) “. Hoci v časti hlásenia úmrtia je uvedené vyhlásenie „Nie“, v časti hlásenia uzdravenia je uvedené aj „Nie“ – to znamená, že dieťa sa neprebralo. Čo sa s ňou potom stalo? Žije alebo zomrela?
Viac ako 1,3 milióna nežiaducich udalostí po očkovaní proti COVID nahlásených VAERS, CDC Data Show
Okrem toho táto správa, podobne ako mnohé iné, vyvoláva niekoľko zložitých otázok. Ako dostalo 43-dňové dieťa vakcínu, ktorá ešte nebola schválená na použitie u dojčiat? Okrem toho sa predpokladá, že súčasné uskutočnené klinické štúdie budú zahŕňať dojčatá a deti staršie ako 6 mesiacov. Bolo toto dieťa účastníkom procesu spoločnosti Pfizers? Správa na túto otázku neodpovedá.
Rovnako ako u tohto bábätka sa ukázalo, že vo väčšine hlásených prípadov bolo u toho istého bábätka zaznamenaných niekoľko život ohrozujúcich vedľajších účinkov. Najčastejšími závažnými nežiaducimi účinkami boli nebezpečné krvácanie; anafylaktický šok – život ohrozujúca alergia, ktorá môže poškodiť dýchací systém a spôsobiť závraty, mdloby a dokonca smrť; anticholinergný syndróm - stav, ktorý sa vyskytuje, keď sú blokované receptorové miesta pre neurotransmiter acetylcholín, čo môže viesť k problémom s koordináciou, zrýchlenej srdcovej frekvencii a iným symptómom; encefalitída – infekcia mozgu, ktorá môže spôsobiť bolesti hlavy, vracanie, stratu vedomia a smrť; hypoglykémia – veľmi nízka hladina cukru v krvi, stav, ktorý môže u dojčiat rýchlo eskalovať až k smrti; a neuroleptický syndróm – ktorý je tiež život ohrozujúci a môže poškodiť srdcové svaly, iné svaly,
Zo súhrnu zistení analýzy podľa vekových a rodových skupín vyplýva nasledujúci obraz:
Vo vekovej skupine 0-6 mesiacov – 28 hlásení, z toho 10 mužov, 16 žien a 2 neuvedené pohlavie.
9 z nich (32 %) malo anticholinergný syndróm, 9 (32 %) malo anafylaktický šok, 8 (28,6 %) malo neuroleptický syndróm, 5 trpelo nepravidelnosťami srdcového rytmu a 5 malo hypoglykémiu.
Vo vekovej skupine 6-12 mesiacov – v tejto skupine bolo zistených 5 hlásení – 3 muži, jedna žena a jedno bez uvedenia pohlavia. Táto skupina je malá v porovnaní s ostatnými skupinami. Zoznam nežiaducich reakcií zahŕňal: anafylaktický šok, anticholinergný syndróm a neuroleptický syndróm.
Vo vekovej skupine od 1 do 3 rokov – v tejto skupine bolo hlásených 25 prípadov, z toho 5 mužov, 19 žien a 1 bábätka bez bližšieho určenia pohlavia.
6 detí (24 %) malo anafylaktický šok, 6 (24 %) malo anticholinergický syndróm, 5 (20 %) malo neuroleptický syndróm, 4 (16 %) trpelo encefalitídou, 3 (12 %) malo nepravidelný srdcový tep, jedno dieťa krvácalo a jedno trpelo hypoglykémiou.
Je potrebné poznamenať, že vyššie uvedené nežiaduce udalosti sú len niektoré z tých, ktoré boli hlásené vo VAERS v súvislosti s dojčatami. Rozhodli sme sa zamerať len na život ohrozujúce a bežné nežiaduce udalosti.
Tabuľka č. 1: Analýza hlásení podľa veku a pohlavia
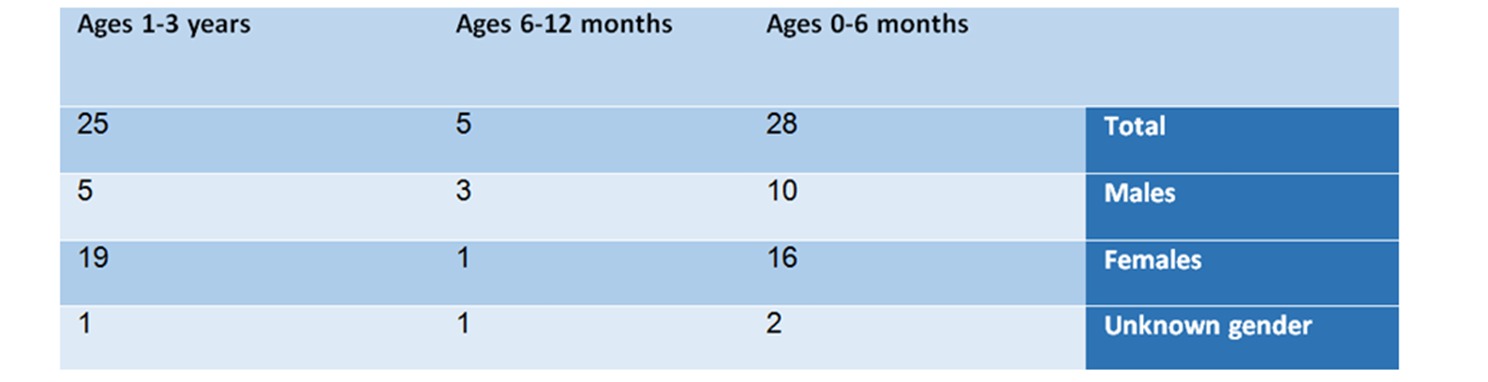
Tabuľka č. 2: Analýza hlásení podľa nežiaducich udalostí
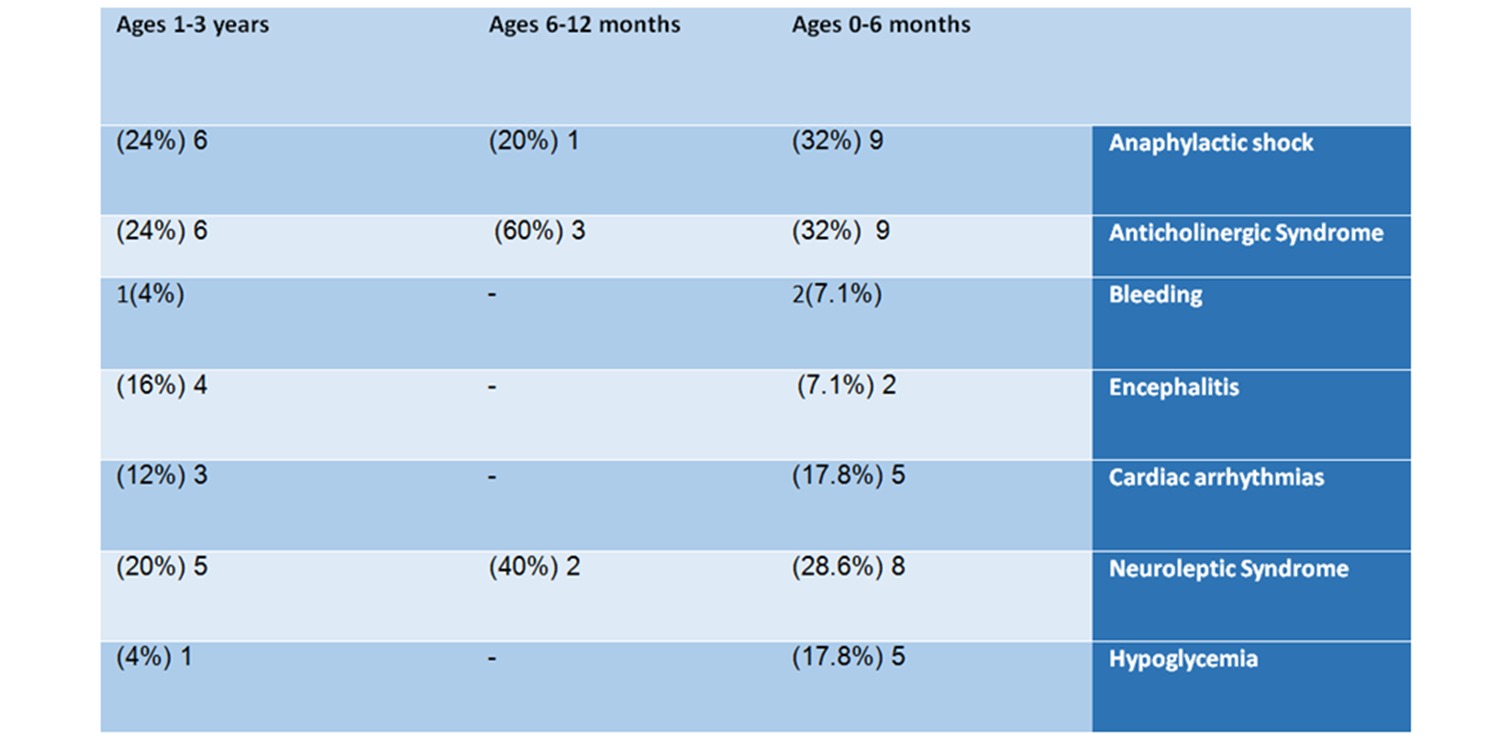
Sú deti živé?
Podobne ako v predchádzajúcom opísanom prípade, ďalšie dvojmesačné bábätko tiež prešlo anafylaktickým šokom po tom, čo bolo 6. januára 2021 vystavené jednej dávke vakcíny Pfizer-BioNTech a rovnako ako ona, podľa správy (č. 976433), trpela radom multisystémových symptómov. Čo sa týka spôsobu podania vakcíny, bolo uvedené „nešpecifikovanou cestou podania“ , čo znamená, že nie je jasné, za akých okolností bolo dieťa vakcíne vystavené.
Bola súčasťou klinickej štúdie spoločnosti Pfizers? Zo správy to opäť nie je jasné.
Dôležitejšou otázkou, ktorú si treba položiť, rovnako ako v predchádzajúcom prípade, je však to, čo sa stalo bábätku? Prežila? je živá?
A opäť, v časti hlásenia smrti je uvedené „Nie“, čo znamená, že dieťa nezomrelo. V popise správy sa však uvádza: „Pacient sa z udalosti nezotavil. Nie sú možné žiadne následné pokusy. Nečakajú sa žiadne ďalšie informácie."
Je ťažké uveriť, ale táto základná otázka – čo sa stalo s bábätkom po takých závažných a život ohrozujúcich nežiaducich reakciách – vyplýva aj z iných závažných prípadov, ako je prípad 6-mesačného bábätka (správa č. 2084418 ), ktorí 29. decembra 2021 „dostali bnt162b2 (COMIRNATY), intramuskulárne“ a prekonali anafylaktický šok, anticholinergný syndróm, neuroleptický syndróm, infekčnú pneumóniu, iné infekcie a multisystémové symptómy.
Aj v tomto prípade je v časti hlásenia úmrtia uvedené „Nie“, čo znamená, že dieťa údajne nezomrelo, zatiaľ čo v popise udalosti sa uvádza „výsledok „neznámy“... Nie sú možné žiadne následné pokusy. Nepredpokladajú sa žiadne ďalšie informácie."
V inom prípade (správa č. 1012508) sa u ročného dieťaťa, ktoré tiež dostalo očkovaciu látku Pfizer, 19. januára 2021 (v tomto prípade je uvedené, že dieťa sa nezúčastnilo pokusu) objavila bolesť. ľavého ucha, ktoré sa vystupňovalo do úplnej paralýzy, ktorá bola diagnostikovaná ako Guillain Barreov syndróm. V popise prípadu bolo uvedené, že dieťa trpelo Guillain Barre syndrómom, ochrnutím tváre, neinfekčnou encefalitídou, neinfekčnou meningitídou, bolesťami uší a poruchami sluchu. Napriek tomu v súhrne správy bolo opäť napísané, že „Nie sú možné žiadne následné pokusy“.
A ďalší šokujúci prípad (číslo správy 1379484) sa vynára zo správy o bábätku, ktoré malo iba jeden mesiac a ktoré utrpelo „vaginálne krvácanie/neustále silné vaginálne krvácanie s kúskami zrazeniny“ nasledujúci deň po tom, čo v máji dostalo vakcínu Pfizer-BioNTech. 19, 2021.
Hoci symptómy, ktorými dieťa trpelo, boli definované ako „závažné až medicínsky významné“ , v popise incidentu sa uvádza, že výsledok je „neznámy“ a že „Nie sú možné žiadne ďalšie pokusy. Nepredpokladajú sa žiadne ďalšie informácie."
Ako už bolo spomenuté, v niektorých prípadoch sa uvádza, že deti neboli súčasťou klinického skúšania, zatiaľ čo v iných nie je jasné, či sa zúčastnili na klinickom skúšaní alebo boli očkované za iných neznámych okolností. Ale či už boli súčasťou procesu alebo nie, správa nevysvetľuje absenciu týchto kritických informácií; čo sa stalo s týmito bábätkami? Prežili? A ak áno, zotavili sa? Prečo sa nesledoval zdravotný stav bábätiek, ktoré trpeli závažnými a život ohrozujúcimi nežiaducimi udalosťami, pričom bolo jasne uvedené, že sa neuzdravili? Nevyžaduje FDA v takýchto závažných prípadoch, aby spoločnosť vynaložila maximálne úsilie na lokalizáciu týchto detí, zistila, aký je ich stav a sledovala ich?
"Sčervenanie v oblasti injekcie: protokol klinickej štúdie nespomína závažné nežiaduce reakcie"
Tlačová správa vydaná 11. februára 2022, v ktorej spoločnosť Pfizer-BioNTech oznámila, že má v úmysle požiadať FDA o schválenie pre dojčatá vo veku od 6 mesiacov do 4 rokov, bezpečnostné zistenia z klinických skúšok spoločnosti u dojčiat a batoliat na tieto veky sa nespomínajú ani slovom. Informačná brožúra týkajúca sa klinických štúdií testujúcich bezpečnosť a účinnosť vakcíny Pfizer u dospelých, detí a dojčiat na webovej stránke FDA, jasne uvádza „Na stránke ClinicalTrials.gov neboli pre túto štúdiu uverejnené žiadne výsledky štúdie“. A ako je uvedené vyššie, novo vydaný dokument The VRBPAC Briefing Document uvádza iba niekoľko nezávažných nežiaducich udalostí hlásených v tejto vekovej skupine, vrátane záverov, že neexistuje nič, čo by naznačovalo nové bezpečnostné obavy. Ako mohol FDA nevedieť o toľkých závažných nežiaducich udalostiach, ktoré boli hlásené do systémov hlásenia CDC? Prípadne, ak o nich vedia – prečo ich ignorujú?
Ako boli testované nežiaduce udalosti u detí v porovnaní s klinickými skúškami? V snahe odpovedať na túto kritickú otázku zameranú na riešenie bezpečnostných problémov a uistenie rodičov, že vakcína je pre deti bezpečná, sme preskúmali protokol štúdie, ktorý sa nachádza na webovej stránke klinickej štúdie FDA.
Zdá sa, že neboli uvedené žiadne potenciálne závažné nežiaduce udalosti. Zoznam potenciálnych nežiaducich udalostí, ktoré mala štúdia vyhodnotiť podľa protokolu („meranie výsledku“), zahŕňal lokálne aj systémové reakcie. Ide však o relatívne nezávažné nežiaduce udalosti.
Zoznam lokálnych nežiaducich účinkov, ktoré mala štúdia monitorovať, zahŕňa: „Bolesť alebo citlivosť v mieste vpichu, začervenanie a opuch“ a systematické reakcie zahŕňali „Horúčku, únavu, bolesť hlavy, zimnicu, vracanie, hnačku, nové alebo zhoršené bolesť svalov, nová alebo zhoršená bolesť kĺbov, znížená chuť do jedla, ospalosť a podráždenosť“. Navyše, hoci sa štúdia plánuje skončiť až 14. júna 2024, časový rámec stanovený na skúmanie nežiaducich účinkov je obmedzený na sedem dní po každej z dávok – prvej a druhej dávke.
Vakcína je u dojčiat neúčinná. Riešenie: znížte prah účinnosti a pridajte tretiu dávku
Okrem vážnych obáv týkajúcich sa bezpečnosti vakcín pre dojčatá je ich účinnosť v tejto vekovej skupine celkovo otázna. Podľa dostupných údajov majú zdravé deti takmer nulové riziko závažných ochorení, hospitalizácie alebo úmrtia v dôsledku COVID-19.
Hospitalizácia v dôsledku COVID-19 je medzi deťmi veľmi zriedkavá a prípady úmrtia sú ešte zriedkavejšie. Napríklad v Nemecku veľká štúdia zistila, že ani jedno dieťa nezomrelo na COVID-19 vo vekovej skupine 5-11 rokov bez predchádzajúcich ochorení. Za týchto okolností je aj jeden prípad závažnej nežiaducej udalosti, nehovoriac o smrti, kľúčový a prevažuje nad možným prínosom vakcíny.
Nie je prekvapením, že klinické štúdie spoločnosti Pfizer u detí mladších ako 4 roky dokázali, že 2 dávky vakcíny významne nezvýšia počet ich protilátok. Komisárka FDA, Dr. Janet Woodcocková, v rozhovore začiatkom apríla 2022 priznala, že „vyvinuté protilátky neboli také vysoké, takže u starších detí nemali rovnakú protilátkovú odpoveď na sériu dvoch dávok. Nebola taká vysoká, ako by sme dúfali u mladších, ako u starších detí.“ Podľa Woodcocka to je dôvod, prečo spoločnosť Pfizer, ktorá plánovala požiadať o schválenie EUA pre dojčatá vo februári, posunula dátum podania a rozhodla sa pridať tretiu dávku do štúdie a počkať na zistenia, keď všetky deti dostanú svoju tretiu dávku.
Okrem toho vo vyhlásení z 11. mája Dr. Peter Marks, riaditeľ Centra pre biologické hodnotenie a výskum pri FDA, oznámil, že vakcíny pre dojčatá a batoľatá nebudú musieť presiahnuť 50 % účinnosť proti Covidu. 50 % účinnosť je hranica, ktorú musia vakcíny pre dospelých prekonať. Marks však vysvetľuje, že napriek predchádzajúcim usmerneniam FDA neodmietne spoločnostiam schválenie pre dojčatá a batoľatá len preto, že nedosiahla 50% účinnosť pri prevencii symptomatických infekcií.
Spoločnosť Pfizer vydala 23. mája tlačovú správu , v ktorej oznámila, že „účinnosť vakcíny 80,3 % bola pozorovaná pri opisnej analýze troch dávok v čase, keď bol Omicron prevládajúcim variantom“. Podľa tlačovej správy „Štúdia naznačuje, že nízka 3-ug dávka našej vakcíny..., poskytuje malým deťom vysokú úroveň ochrany proti nedávnym kmeňom COVID-19“.
Napriek tomu informačný dokument FDA odhaľuje, že nárok na „vysokú úroveň ochrany“ je založený na celkovo 10 symptomatických prípadoch COVID-19 identifikovaných v štúdii, ktoré sa vyskytli najmenej 7 dní po dávke 3. Tri z nich sa vyskytli medzi účastníkmi vo veku 6 – 23 mesiacov vek (ktorý zahŕňal 555 účastníkov – 376 v skupine s vakcínou a 179 v skupine s placebom) – s 1 prípadom v skupine s vakcínou Pfizer-BioNTech a dvoma v skupine s placebom. Sedem ďalších prípadov sa vyskytlo medzi účastníkmi vo veku 2 až 4 roky (ktoré zahŕňali 860 účastníkov – 589 v skupine s vakcínou a 271 v skupine s placebom) – s 2 prípadmi v skupine s vakcínou Pfizer-BioNTech v porovnaní s 5 v skupine s placebom. Napriek tomu bola účinnosť vakcíny FDA stanovená na 80,4 %, a v dokumente sa uvádza, že „Dostupné údaje podporujú účinnosť 3-dávkovej primárnej série vakcíny Pfizer-BioNtech COVID-19 (3 µg každá dávka) pri prevencii COVID-19 vo vekovej skupine od 6 mesiacov do 4 rokov“. Okrem toho sa v dokumente uvádza, že „Medzi dojčatami a deťmi vo veku od 6 mesiacov do 4 rokov je miera hospitalizácií a úmrtí v dôsledku COVID-19 vyššia ako u detí a dospievajúcich vo veku 5-17 rokov a porovnateľná s jednotlivcami vo veku 18- 25 rokov, čo podčiarkuje prínos účinnej vakcíny proti COVID19 v tejto vekovej skupine.
Aké etické je dať zaočkovať dieťa proti chorobe, pri ktorej je šanca, že ťažko ochorie alebo na ňu zomrie, takmer nulová, zatiaľ čo prínosy liečby sú nejasné a nežiaduce reakcie ohrozujúce život sú veľmi významné?
Táto otázka bola témou článku publikovaného v marci tohto roku v Bioetike . Výskumníci uviedli, že ani jedno z hlavných tvrdení, ktorými sa ospravedlňuje schválenie pre bábätká, nie je platné. Podľa nich je prínos vakcíny pre zdravé deti minimálny, a preto, aj keď sú komplikácie zriedkavé, prevažujú nad prínosom vakcíny, najmä preto, že je veľmi nejasné, aké sú krátkodobé a dlhodobé riziká a skúsenosti s vakcína je veľmi krátka. Altruistické tvrdenie o ochrane životného prostredia je tiež veľmi problematické, keďže ako vakcína existuje, ohrozené skupiny sa vedia brániť a už sa dokázalo, že deti nie sú hlavnými prenášačmi vírusu.
Členovia kongresu požadujú odpovede
Tento etický problém nastolilo v posledných dňoch 18 členov Kongresu v liste zaslanom FDA 7. júna, v ktorom žiadajú odpovede pred rozhodnutím úradu udeliť núdzové povolenie pre vakcínu pre dojčatá. Členovia Kongresu požadovali vedieť, prečo sú vakcíny COVID-19 potrebné pre túto vekovú skupinu vzhľadom na skutočnosť, že choroba predstavuje veľmi malé riziko pre dojčatá a malé deti, že vakcíny sú málo účinné a že existuje veľa nezodpovedaných otázok týkajúcich sa bezpečnosť a nežiaduce účinky týchto vakcín.
V liste sa FDA predkladá 19 otázok, medzi inými – prečo FDA odložila zverejnenie stoviek tisíc strán s údajmi zo štúdií výrobcov, stav nežiaducich udalostí a kedy možno očakávať, že všetky údaje FDA budú byť zverejnené? FDA bola tiež požiadaná, aby verejnosti poskytla ďalšie podrobnosti o deťoch, ktoré boli vážne zranené alebo zomreli na COVID-19, a o tom, koľko detí vo všeobecnosti vážne ochorelo. Zákonodarcovia sa tiež zaoberali otázkou kardiálnych rizík pri podávaní vakcín mRNA COVID-19 deťom, pričom poznamenali, že po očkovaní veľkého počtu detí vo veku 5-18 rokov bol pozorovaný nárast myokarditídy a perikarditídy, pričom niektoré prípady končili smrťou, a dlhodobé účinky zápalu súvisiaceho so srdcom, ktoré zdravotnícke orgány ešte nekvantifikovali. Čo je viac,

FDA nebude môcť tvrdiť, že nevedel
Ako už bolo uvedené, údaje vyplývajúce z analýzy prezentovanej v tomto článku bez akýchkoľvek pochybností preukazujú, že vakcína nie je bezpečná pre dojčatá a batoľatá. Či už boli tieto deti súčasťou štúdie alebo nie – tieto správy sú v systéme VAERS už mnoho mesiacov, takže nie je šanca, že ich FDA nepozná. Bohužiaľ, skutočnosť, že FDA vedela aspoň o niektorých závažných nežiaducich udalostiach, vrátane zvýšeného rizika chorobnosti v prvých dňoch po očkovaní, myokarditídy a zvýšeného rizika potratu a malformácií plodu, a napriek tomu schválila vakcínu pre dospievajúcich, deti a tehotné ženy, bol neskôr odhalený príliš neskoro – dlho po udelení EUA spoločnostiam Pfizer a Moderna, keď už mnohí boli poškodení. Vyjasnilo sa to až vďaka žiadostiam FOIA (Freedom of Information) predloženým FDA a iným zdravotníckym orgánom a až potom, čo bol FDA súdom prinútený zverejniť dokumenty. Tentoraz tu uvedené údaje VAERS umožňujú odhaliť túto skutočnosť ešte pred kolaudáciou. FDA nebude môcť tvrdiť, že nevedel.
Zdroj:www.globalresearch.ca




