{jcomments off}Zatiaľ čo stále viac krajín presadzuje takzvané „posilňovacie“ očkovanie a chce ho dokonca zaviesť ako povinné, Svetová zdravotnícka organizácia (WHO) ich kritizuje. Neexistujú „žiadne dôkazy“, že tieto poskytujú „väčšiu ochranu“ pre zdravých ľudí
Svetová zdravotnícka organizácia spochybnila rozhodnutie vlády Spojeného kráľovstva distribuovať medzi obyvateľstvo stovky miliónov posilňujúcich očkovaní a tvrdila , že neexistuje „žiadny dôkaz“, že by tieto očkovania poskytovali „väčšiu ochranu“ zdravým. Zjavne sa to prenieslo aj do WHO, že nemá zmysel „posilňovať“ zdravých ľudí experimentálnymi vakcínami, ktoré aj tak nie sú zamerané na aktuálne cirkulujúce varianty.
Minister zdravotníctva Spojeného kráľovstva Sajid Javid uviedol, že krajina zabezpečila ďalších 114 miliónov dávok vakcíny na roky 2022 a 2023, aby si „kúpila čas“, a do konca januára ponúkne očkovanie všetkým starším ako 18 rokov. DR. Mike Ryan, riaditeľ núdzového programu WHO, spochybnil dôvod tohto rozhodnutia. "V tejto chvíli, pokiaľ je mi známe, neexistujú žiadne dôkazy o tom, že posilnenie populácie ako celku by nevyhnutne poskytlo väčšiu ochranu inak zdravým ľuďom pred hospitalizáciou a smrťou," povedal.
Angličania chcú stále zaočkovať viac detí
Ryan tiež poznamenal, že Spojené kráľovstvo je v „luxusnej pozícii“ v tom, že môže ponúknuť posilňovacie očkovanie celej svojej populácii, keďže mnohé chudobnejšie krajiny ani nemajú vakcíny, ktoré by dali dávku každému. Tu môžete vidieť, že WHO naďalej presadzuje, aby sa tieto experimentálne vakcíny distribuovali po celom svete.
Zdravotnícke úrady Spojeného kráľovstva medzitým prijali variant Omicron, aby vyzvali viac detí, aby sa dali zaočkovať. Je to zvláštne, pretože je známe, že tento variant spôsobuje iba „mierne“ symptómy, najmä u mladšej populácie. Odborníci tvrdia, že je nebezpečné odmietnuť Omicron ako „mierny“, pretože Južná Afrika má veľmi mladú populáciu (priemerný vek 27 rokov) a nevieme, ako táto choroba ovplyvní starších ľudí. Riešením je vraj zaočkovať viac mladších ľudí. To dáva perfektný zmysel... nie?
Sú takéto „posilňovacie očkovania“ nebezpečné?
Ak si uvedomíte, že oficiálne údaje WHO už ukazujú množstvo vedľajších účinkov, mnohí ľudia si kladú otázku, ako môžu takéto „predplatné riešenia“ s preočkovaním vôbec fungovať. Hovoríme o tom, že tieto experimentálne vakcíny (kritickí lekári správne nazývajú injekčné striekačky mRNA „génová terapia“) spôsobujú poškodenie niekoľko týždňov po každom podaní. Napríklad imunitný systém je ovplyvnený vakcínami (1). Výsledok: Stále viac ľudí môže zomrieť na skutočne jednoduché choroby. Nehovoriac o všetkých vedľajších účinkoch (pozri správu WHO (2) alebo VAERS (3)).
Ak si tiež uvedomíte, že vlády s radosťou odporúčajú mRNA vakcíny Pfizer na takéto „posilňovacie“ injekcie, hoci táto veľká farmaceutická spoločnosť a americký FDA vedeli o mnohých vedľajších účinkoch už od začiatku roka, ukazuje sa, že prečo je vo svete tlak na ďalšiu administratívu. Koná sa podľa hesla: Západný svet je z veľkej časti zaočkovaný, teraz sú na rade chudobné a rozvíjajúce sa krajiny, kým sa celé strašidlo skončí? Darebák, ktorý to zle myslí. Pretože napríklad v Afrike nie sú takmer žiadne problémy s Covidom - ale ak oslabíte imunitnú obranu pomocou experimentálnych vakcín, mohli by ste spôsobiť, že desiatky miliónov ľudí budú náchylné na mnohé patogény.
WHO spochybňuje britskú politiku posilňovacej vakcíny
Poznamenajúc, že toto bola „luxusná pozícia“, kým iné krajiny nemajú dostatok vakcín na ochranu svojich najzraniteľnejších, Dr. Mike Ryan – vedúci núdzového programu agentúry – v stredu povedal, že to bolo „ťažké pre niektoré krajiny, ktoré obrovské množstvo prebytočnej vakcíny, aby sa rozhodlo, komu ju dať.“
Jeho komentáre prišli pred štvrtkovým vyhlásením ministra zdravotníctva Spojeného kráľovstva Sajida Javida, že krajina zabezpečila ďalších 114 miliónov dávok vakcíny na roky 2022 a 2023, aby si „kúpila čas“, keďže sa zaoberá prípadmi nového variantu vírusu Omicron. Začiatkom týždňa vláda oznámila, že každému nad 18 rokov bude do konca januára ponúknutá posilňovacia dávka.
Javid zopakoval, že vakcíny „stále zostávajú našou najlepšou obrannou líniou“, povedal Javid, že dohody – ktoré údajne zahŕňajú 60 miliónov dávok vakcíny Moderna a 54 miliónov pichnutí Pfizerom – zabezpečia krajine dostatok vakcín, „ktoré potrebujeme z dlhodobého hľadiska. “
Ryan poznamenal, že vlády by sa mali zamerať na svoju epidemiologickú situáciu pred blížiacim sa sviatočným obdobím, no kritizoval programy posilňovacej vakcinácie aj krajiny plánujúce variant Omicron, zatiaľ čo v Európe bola „kríza... poháňaná variantom Delta“.
Momentálne neexistuje žiadny dôkaz, o ktorom by som vedel, že by naznačovalo, že posilnenie celej populácie by nevyhnutne poskytlo väčšiu ochranu inak zdravým jedincom pred hospitalizáciou a smrťou.
V rámci nového programu Spojeného kráľovstva Javid uviedol, že obdobie medzi druhými dávkami a posilňovacími injekciami sa skráti zo šiestich na tri mesiace a dodal, že deťom vo veku 12 až 15 rokov bude ponúknutá druhá dávka po troch mesiacoch.
Medzitým by ľudia s vážnymi nedostatkami imunitného systému mohli dostať ďalšiu posilňovaciu vakcínu, vďaka ktorej by niektorí jedinci dostali štvrtú dávku.
(1)Poškodenie imunitného systému: štúdie varujú pred následkami očkovaniu
Očkovanie proti Covidu zrejme spôsobuje útok na imunitné bunky ľudského tela. Ukazujú to údaje z novej štúdie. V opačnom prípade sú všetky vedľajšie účinky mimoriadne znepokojujúce. Ako dlho to ešte bude fungovať? Vytvárame svet plný chronicky chorých ľudí?
„ Rozsiahle štúdie preukázali konzistentné patofyziologické zmeny po očkovaní vakcínami proti Covid-19, (4)“ je názov štúdie, ktorá bola publikovaná v časopise „Nature“. Vedecké výsledky sú znepokojujúce. Pretože scRNA-seq vykazovala po očkovaní dramatické zmeny v génovej expresii takmer všetkých imunitných buniek.
Tvorba neutralizačných protilátok bola stanovená prostredníctvom konzistentných zmien hemoglobínu A1c, hladín sodíka a draslíka v sére, koagulačných profilov a funkcií obličiek u zdravých dobrovoľníkov po očkovaní inaktivovanou vakcínou proti SARS-CoV-2 (Sinopharm). Podobné zmeny boli hlásené aj u pacientov s Covid-19. To naznačuje, že očkovanie napodobňuje infekciu. Jednobunkové sekvenovanie mRNA (scRNA-seq) mononukleárnych buniek periférnej krvi (PBMC) pred a 28 dní po prvej inokulácii tiež ukázalo konzistentné zmeny v génovej expresii mnohých rôznych typov imunitných buniek. Redukcia CD8 + T buniek (pozn. redakcie: imunitné bunky) a zvýšenie klasickej hladiny monocytov boli obrovské.
Rovnako ako pri infekciách Covid
Očkovanie má podľa vedcov na organizmus podobné účinky ako samotný Covid, okrem iného výrazne klesá hladina draslíka v krvnom sére a narúša sa rovnováha elektrolytov. Návrat k normálnym hodnotám bolo možné určiť až po 90 dňoch. Je to pravdepodobne spôsobené aj tým, že vakcíny ponúkajú aj tak len základnú ochranu na niekoľko mesiacov. Zistila sa však aj zvýšená hladina cholesterolu a zvýšená celková hladina žlčových kyselín. Okrem toho došlo k dysfunkcii obličiek. Všetky príznaky, ktoré sú spojené so závažnými ochoreniami Covid 19.
Aby sa objasnilo, či sa tieto výsledky dajú aplikovať rovnako na všetky vakcíny proti Covid, podľa autorov sú stále potrebné zodpovedajúce štúdie. Analýzy uskutočnené v rámci štúdie by podľa vedcov mali v najlepšom prípade patriť do štandardného repertoáru pri vývoji vakcín, pretože s takýmito negatívnymi účinkami vakcín na ľudské zdravie treba rátať už pred použitím – vlastne. Našlo sa tu totiž, že údajne „chránilo“ ľudí po očkovaníPo pravde, aspoň na krátky čas (28 dní) po výstrele sa zdá, že majú oslabený imunitný systém a potrebujú tak väčšiu ochranu ako bez očkovania. Krátkodobé protilátky proti Covid-19 môžu tento negatívny efekt len ťažko kompenzovať.
Spike proteín zhoršuje adaptívny imunitný systém
V skutočnosti sa v októbri v časopise „Viruses“ objavila štúdia, ktorá preukázala škodlivé účinky vrcholových proteínov SARS-CoV-2 na imunitný systém in vitro. V súlade s tým spike proteíny inhibujú opravu poškodenia DNA, čo je nevyhnutné pre účinnú V(D)J rekombináciu - mechanizmus, ktorý je nevyhnutný pre adaptívny imunitný systém. Pre výskumníkov to jednoznačne vedie k negatívnemu účinku tých vakcín založených na spike proteíne, ktorý je naliehavo potrebné preskúmať. Prvé vedecké dôkazy o škodlivých účinkoch vakcín Covid používaných v tejto krajine na imunitný systém sú už k dispozícii.
Záver
Opäť sa ukazuje, že experimentálne vakcíny Covid mali byť podrobené oveľa podrobnejším analýzam a vyšetrovaniam predtým, ako boli uvoľnené pre bežnú populáciu. Už predtým známe, niekedy vážne vedľajšie účinky u očkovaných osôb to ukázali. Možnosť, že mRNA vakcíny používané v tejto krajine majú tiež negatívny vplyv na imunitný systém očkovaných osôb, musí byť kriticky spochybnená a preskúmaná – v neposlednom rade preto, že už tak základný ochranný účinok všetkých schválených vakcín rýchlo vyprchá a s každou vakcínou sa objaví nová. - tzv. posilňovacia vakcinácia, môže dôjsť k potenciálnemu útoku na ľudský imunitný systém.
(4) https://www.nature.com/articles/s41421-021-00329-3
Preklad:
Komplexné výskumy odhalili konzistentné patofyziologické zmeny po očkovaní vakcínami COVID-19
Abstraktné
V súčasnosti prebiehajú rozsiahle očkovania proti COVID-19 v mnohých krajinách v reakcii na pandémiu COVID-19. Tu uvádzame okrem vytvárania neutralizačných protilátok aj konzistentné zmeny hemoglobínu A1c, sérových hladín sodíka a draslíka, koagulačných profilov a renálnych funkcií u zdravých dobrovoľníkov po očkovaní inaktivovanou vakcínou proti SARS-CoV-2. Podobné zmeny boli hlásené aj u pacientov s COVID-19, čo naznačuje, že očkovanie napodobňuje infekciu. Jednobunkové sekvenovanie mRNA (scRNA-seq) mononukleárnych buniek periférnej krvi (PBMC) pred a 28 dní po prvej inokulácii tiež odhalilo konzistentné zmeny v génovej expresii mnohých rôznych typov imunitných buniek. Zníženie CD8 +T bunky a zvýšenie klasického obsahu monocytov boli príkladné. Okrem toho scRNA-seq odhalila zvýšenú signalizáciu NF-KB a znížené reakcie interferónu typu I, ktoré boli potvrdené biologickými testami a bolo tiež hlásené, že k nim dochádza po infekcii SARS-CoV-2 so zhoršujúcimi sa symptómami. Naša štúdia celkovo odporúča dodatočnú opatrnosť pri očkovaní ľudí s už existujúcimi klinickými stavmi, vrátane cukrovky, nerovnováhy elektrolytov, renálnej dysfunkcie a porúch koagulácie.
Úvod
Pandémia COVID-19 hlboko zasiahla ľudstvo. Vývoj vakcín proti COVID-19 v rôznych formách prebieha bezprecedentným a zrýchleným spôsobom. Napriek určitým neistotám týkajúcim sa možných následkov sa v mnohých krajinách uskutočňuje rozsiahle očkovanie. Boli vyvinuté rôzne vakcíny COVID-19 vrátane inaktivovaných vírusových častíc, mRNA vakcín, vakcín na báze adenovírusov atď. 1 , 2 , 3 , 4 , 5. Historicky sa výskum vakcín zameriaval na to, či očkovanie môže alebo nemôže generovať neutralizačné protilátky na ochranu pred vírusovými infekciami, zatiaľ čo krátkodobé a dlhodobé vplyvy rôznych novo vyvinutých vakcín na ľudskú patofyziológiu a iné perspektívy ľudského imunitného systému to nedokázali. plne preskúmané.
S vývojom technológie sekvenovania mRNA vo veľkom meradle (scRNA-seq) bolo možné systematické skúmanie funkcie ľudského imunitného systému s presnosťou, predovšetkým prostredníctvom scRNA-seq mononukleárnych buniek periférnej krvi (PBMC). Počas pandémie COVID-19 veľké množstvo štúdií s použitím scRNA-seq PBMC odhalilo podrobné zmeny v génovej expresii v rôznych podtypoch imunitných buniek vrátane rôznych typov T a B buniek, NK buniek, monocytov, dendritických buniek atď. a po infekcii, výsledky, z ktorých vyplývajú značne znížené CD4 + a CD8 +Počet T-buniek a vyčerpanie T-buniek po infekcii SARS-CoV-2. Pozoroval sa aj znížený počet periférnych slizničných nemenných T (MAIT) buniek a ich migrácia do az pľúc. U pacientov s COVID-19 boli hlásené vysoko aktivované zápalové imunitné reakcie, vrátane reakcií na interferón-gama (IFN-γ), interleukín-6 (IL-6) a NF-κB 6 , 7 , 8 , 9 , 10 , 11 , 12. Mnohé štúdie odhalili rozdiely v imunitnom stave medzi ľuďmi so závažnými a miernymi príznakmi v tom, že silné reakcie interferónu typu I (IFN-α/β) boli prospešné po infekcii COVID-19 a oslabené reakcie IFN-α/β boli spojené s rozvojom ťažké príznaky 13 . Na rozdiel od toho, silnejšie zápalové reakcie NF-KB boli spojené so závažnejšími symptómami 14 . Okrem toho sa uvádza, že zvýšený obsah γδ-T buniek a znížený obsah neutrofilov sú spojené s miernejšími symptómami 15 .
Po infekciách SARS-CoV-2 sa u mnohých ľudí vyvinuli rôzne stupne respiračných syndrómov a niektorí s gastrointestinálnymi ochoreniami. Bolo hlásené, že poruchy zrážanlivosti krvi, problémy s vaskulatúrou, nerovnováha elektrolytov, poruchy obličiek, metabolické poruchy atď. sú hlavnými klinickými komplikáciami COVID-19 16 , 17 . Spôsob, akým by očkovanie napodobňovalo infekciu, nebol úplne vyhodnotený. Do tejto štúdie sme zaradili zdravých dobrovoľníkov, ktorí mali byť očkovaní inaktivovanou vakcínou proti SARS-CoV-2 (Vero Cell) 3, zúčastniť sa testovania protilátok a neutralizujúcich protilátok, ako aj podrobných klinických laboratórnych meraní pred a v rôznych časoch po očkovaní (aplikovali sa dvojdávkové režimy s mierne odlišnými schémami). Na naše prekvapenie sme pozorovali celkom konzistentné patofyziologické zmeny týkajúce sa obsahu elektrolytov, koagulačných profilov, funkcie obličiek, ako aj metabolických vlastností cholesterolu a glukózy, ako keby títo ľudia zažili infekciu SARS-CoV-2. Okrem toho výsledky scRNA-seq PBMC tiež ukázali konzistentné zníženie CD8 +T bunky a zvýšenie obsahu monocytov, ako aj zvýšená zápalová signalizácia NF-KB, ktorá tiež napodobňovala reakcie po infekcii. Prekvapivo sa reakcie na interferón typu I, ktoré boli spojené so zníženým poškodením po infekcii SARS-CoV-2 a miernejšími symptómami, zdali byť po očkovaní znížené, aspoň 28 dní po prvom očkovaní. To by mohlo naznačovať, že krátkodobo (1 mesiac) po očkovaní je imunitný systém osoby v neprivilegovanom stave a môže vyžadovať väčšiu ochranu.
Výsledky
Dlhodobé sledovanie produkcie protilátok proti SARS-CoV-2 a neutralizujúcich protilátok po naočkovaní inaktivovanej vakcíny proti SARS-CoV-2
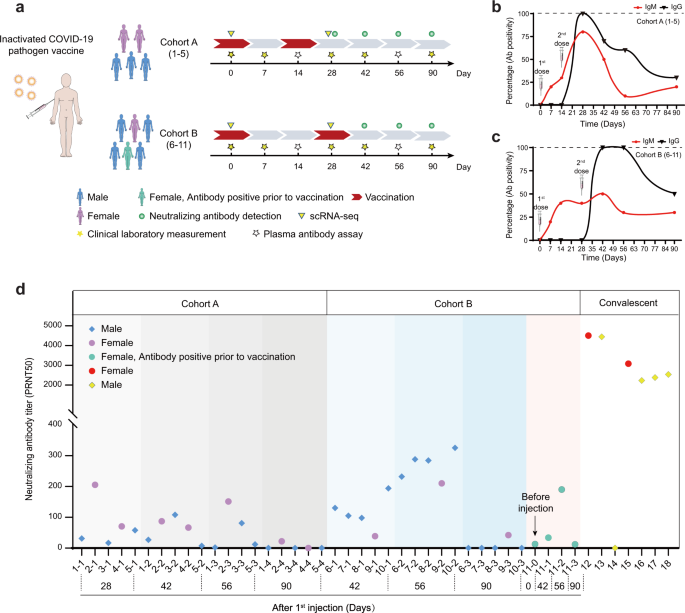
Do tejto štúdie bolo zaradených celkom 11 zdravých dospelých dobrovoľníkov oboch pohlaví vo veku 24–47 rokov s BMI 21,5–30,0 kg/m² (obr. 1a a doplnkové tabuľky S1 a S2 ). Vakcína SARS-CoV-2 (Vero Cell), inaktivovaná (Beijing Institute of Biological Products Co. Ltd), bola podaná intramuskulárne do deltového svalu. Dobrovoľníci boli rozdelení do dvoch skupín; päť účastníkov (kohorta A) bolo očkovaných plnou dávkou (4 µg) inaktivovanej vakcíny SARS-CoV-2 (Vero Cell) v dňoch 1 a 14 a šesť účastníkov (kohorta B) dostalo plnú dávku vakcíny v dňoch 1 a 28 (obr. la). Jeden z dobrovoľníkov v skupine B bol tesne pred očkovaním pozitívne testovaný na anti-SARS-CoV-2 IgM a IgG, čo naznačuje potenciálne predchádzajúce infekcie. Neexistoval však žiadny záznam o predchádzajúcej pozitivite na základe diagnózy nukleovej kyseliny (NA) na COVID-19 (označené zelenou na Obr. 1a ). Pre všetky následné vyšetrenia boli údaje od tohto jedinca označené zelenou farbou, aby sa sledovali všetky možné vplyvy z potenciálnych predchádzajúcich infekcií.
a Schematický popis stratégií očkovania vakcínou, odbery vzoriek krvi a merania. b , c Zmeny pozitivity protilátok (percento pozitívnych/celkových) v priebehu času v kohortách A a B. Dobrovoľníci v kohorte A boli naočkovaní na 1. a 14. deň a v kohorte B na 1. a 28. deň. Červená čiara predstavuje zmeny IgM a čierna, IgG. d Zmeny neutralizačného titra protilátok v plazme dobrovoľníkov v kohortách A a B po očkovaní, ako aj od testovaných jedincov v rekonvalescencii.
Nežiaduce udalosti sa monitorovali denne počas prvých 7 dní po každej inokulácii a potom si ich účastníci sami zaznamenali do denníkov v nasledujúcich týždňoch. Celkovo boli nežiaduce reakcie mierne (1. alebo 2. stupeň) a prechodné (doplnková tabuľka S3 ). Vzorky krvi sa odoberali v dňoch 0, 7, 14, 28, 42, 56 a 90 a vzorky moču sa odobrali v dňoch 0, 14, 28, 42 a 90. Vzorky plazmy sa podrobili anti-SARS-CoV- 2 IgM/IgG testovanie pomocou viacerých diagnostických súprav, na kvantifikáciu boli použité výsledky z najcitlivejšej súpravy (obr. 1b, c). Výsledky testovania kohorty A ukázali, že pred 2. očkovaním sa u 0 % účastníkov vyvinul anti-SARS-CoV-2 IgG, ale na 28. deň, čo boli 2 týždne po 2. očkovaní, bolo 100 % účastníkov testovaných pozitívne ( Obr. lb ). Celkovo sa IgM objavil skôr ako IgG, čo sa očakávalo. Pozitivita IgG a IgM klesla na 42. deň a zostala na relatívne nízkych hladinách do 90. dňa v kohorte A. V kohorte B sa u nikoho nevyvinul IgG až po 2. inokulácii. Na 42. deň však IgG pozitivita dosiahla 100 % (obr. 1c) a trvala až do dňa 56, čo naznačuje, že vakcinačný protokol pre kohortu B bol účinnejší. Na 90. deň sa pozitivita IgG tiež znížila na 50 %, čo naznačuje, že produkcia protilátok sa dlho neudržala. Ďalej sme vykonali testy na SARS-CoV-2 neutralizujúce protilátky 18 (obr. 1d ) a výsledky tiež ukázali, že dve očkovania s odstupom 28 dní (kohorta B) viedli k vyšším ochranným protilátkovým titrom v porovnaní s dvomi očkovaniami s odstupom 14 dní ( kohorta A). Na druhej strane sa zdalo, že titre neutralizačných protilátok proti SARS-CoV-2 boli celkovo nižšie ako titre u pacientov v rekonvalescencii COVID-19, ako bolo uvedené pred 3 (obr. 1d). Po 90 dňoch sa titre neutralizačných protilátok dramaticky znížili u všetkých dobrovoľníkov (obr. 1d ). Je zaujímavé, že jednotlivec, ktorý bol pred očkovaním pozitívny na protilátky, nebol náchylnejší na tvorbu neutralizujúcich protilátok v porovnaní so zvyškom účastníkov, čo naznačuje, že predchádzajúca potenciálna infekcia sa nemusela vyskytnúť alebo nemusí vytvárať dlhotrvajúcu ochranu z hľadiska neutralizácie. produkciu protilátok.
Zmeny v klinických laboratórnych meraniach po očkovaní
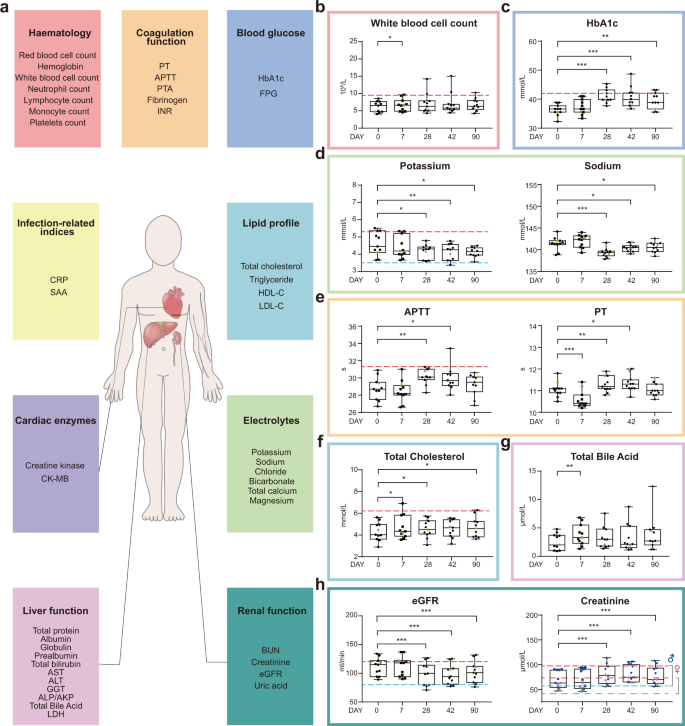
Klinické laboratórne rutinné testy vrátane indexov súvisiacich s infekciou, hematologických parametrov, koagulačnej funkcie, glukózy v krvi, sérových lipidov, enzýmov súvisiacich s funkciou srdca, elektrolytov, biomarkerov súvisiacich s funkciou pečene a obličiek sa merali, aby sa odhalili bezpečnostné vlastnosti vakcíny (obr. . 2a a dodatkové tabuľky S4 a S5 ). Počet bielych krviniek bol významne, ale len mierne zvýšený po očkovaní na 7. deň. V nasledujúcich časových bodoch neboli detekovateľné žiadne rozdiely (obr. 2b). Na naše prekvapenie sa u zdravých dobrovoľníkov pozorovalo celkom konzistentné zvýšenie hladín HbA1c, bez ohľadu na to, či patrili do kohorty A alebo B. Na 28. deň po 1. inokulácii dosiahli tri z 11 jedincov prediabetický rozsah (obr. 2c ). Na 42. a 90. deň sa zdá, že stredné hladiny HbA1c sa vrátili späť, ale stále boli výrazne vyššie ako pred očkovaním. Predchádzajúca práca preukázala, že diabetici s nekontrolovanými hladinami glukózy v krvi sú náchylnejší na rozvoj závažných foriem COVID-19 19 . Ukázalo sa, že vysoké hladiny glukózy v krvi/glykolýza podporujú replikáciu SARS-CoV-2 v ľudských monocytoch prostredníctvom produkcie mitochondriálnych reaktívnych foriem kyslíka a aktivácie HIF1A 20, preto predstavuje nevýhodnú vlastnosť.
a Klinické laboratórne rutinné testy zahŕňajú hematologické a koagulačné parametre, indexy súvisiace s glukózou v krvi a súvisiace s infekciou, lipidový profil, srdcové enzýmy, elektrolyty, biomarkery súvisiace s funkciou pečene a obličiek. Viac informácií možno nájsť v doplnkových tabuľkách S4 a S5 . Laboratórne hodnoty počtu bielych krviniek ( b ), HbA1c ( c ), draslíka ( d , ľavý panel), sodíka ( d , pravý panel), APTT ( e , ľavý panel), PT ( e , pravý panel), celkom cholesterol ( f ), celková žlčová kyselina ( g ), eGFR ( h , ľavý panel), kreatinín ( h, pravý panel). Dátové body predstavujú hodnoty každého jednotlivca. Krabicové grafy ukázali 25., 50. (medián) a 75. percentil. Horizontálne prerušované čiary znázorňujú horné normálne limity (červené) v b , c , d (ľavý panel), e (ľavý panel), f , h a spodné normálne limity (modré) v d (ľavý panel) ah . Hodnoty P sa vypočítali pomocou Wilcoxonovho testu poradia znakov porovnaním laboratórnych meraní v každom čase so základnými meraniami. * P ≤ 0,05, ** P ≤ 0,01, *** P ≤ 0,001.
Hladiny draslíka v sére sa významne znížili na 28., 42. a 90. deň po prvej inokulácii, pričom jedna vzorka bola na 42. deň pod dolnou normálnou hranicou (obr. 2d , ľavý panel). Podobne sa hladiny sodíka v sére tiež znížili po vakcinácii (obr. 2d , pravý panel), čo naznačuje vplyv vakcíny na rovnováhu elektrolytov. S COVID-19 21 opäť súvisí aj nerovnováha elektrolytov . Koagulopatia je ďalší klinický stav vyvolaný COVID-19 22. Zistili sme, že koagulačné profily sa výrazne zmenili po očkovaní, krátkodobo (7 dní) po 1. očkovaní sa koagulačné profily prikláňali ku kratšiemu protrombínovému času (PT), zatiaľ čo dlhodobý (28 a 42 dní) účinok smeroval k aktivovaný parciálny tromboplastínový čas (APTT) a predĺženie PT (obr. 2e ). Na 90. deň sa profily vrátili späť na profily pred očkovaním (obr. 2e ). Okrem toho sme zistili zvýšené hladiny cholesterolu v krvi na 7., 28. deň po 1. očkovaní a zvýšené hladiny celkovej žlčovej kyseliny boli tiež zistené na 7. deň (obr. 2f, g). Renálna dysfunkcia je ďalším klinickým stavom spojeným s COVID-19 a 28., 42. a 90. deň po prvej inokulácii boli hladiny kreatinínu v sére významne vyššie ako pred očkovaním, čo viedlo k zníženiu eGFR (obr. 2h ). Uvádza sa, že väčšina z týchto klinických znakov súvisí s rozvojom závažných symptómov u pacientov s COVID-19 (doplnková tabuľka S6 ). Celkovo neexistovali žiadne štatisticky významné rozdiely medzi kohortami A a B, s výnimkou niekoľkých indexov (doplnková tabuľka S7 ), preto sa údaje z dvoch kohort spojili na prezentáciu klinických údajov a následné analýzy.
scRNA-seq odhalila dramatické zmeny v génovej expresii takmer všetkých imunitných buniek po očkovaní
Aby sme preskúmali imunologické vlastnosti zdravých dobrovoľníkov po očkovaní, vykonali sme kvapôčkovú scRNA-seq (10× Genomics), aby sme študovali transkriptomické profily PBMC od dobrovoľníkov patriacich do kohorty A alebo B, pred a 28 dní po očkovaní (obr. 3a a doplnkový obrázok S1a ). Po predspracovaní a eliminácii buniek nízkej kvality (pozri „Materiály a metódy“) sme získali 188 886 buniek zo všetkých vzoriek PBMC, medzi ktorými bolo 86 685 buniek z kohorty A a 102 201 buniek z kohorty B. Všetky kvalifikované bunky boli integrované do zjednoteného súboru údajov a podrobené následným analýzam.
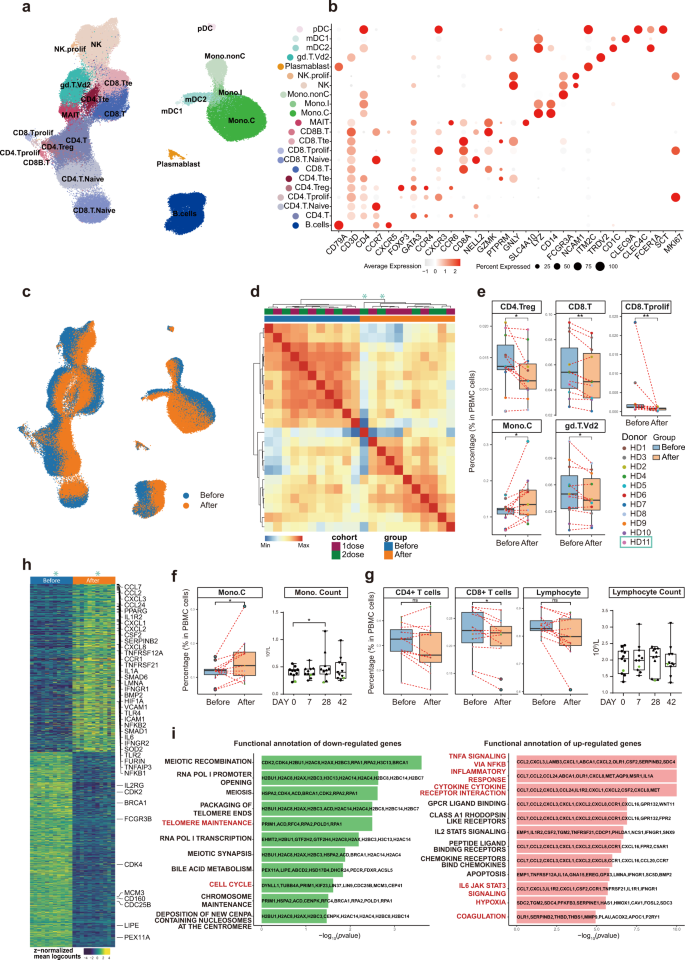
typ buniek UMAP zastúpenie všetkých zlúčené vzoriek. Celkovo bolo identifikovaných 22 bunkových typov pomocou podpisov génovej expresie špecifických pre bunkový typ. Celkovo bolo znázornených 188 886 buniek. b Bodový graf pre gény špecifické pre typ bunky. Farebná škála indikovala úrovne expresie a veľkosť bodu predstavovala percento buniek na klaster/podtyp exprimujúcich zodpovedajúci gén. c UMAP reprezentácia reprezentujúca bunky pred (modrá) a po (oranžová) vakcinácia. d Teplotná mapa korelácie medzi pseudo-hromadnými vzorkami. ePercento špecifických subtypov imunitných buniek v celkových PBMC od každého jednotlivca pred a po očkovaní. Rámčekový graf znázorňoval distribúciu vzorky. Modré rámčeky predstavovali vzorky pred a oranžové po očkovaní. Hodnoty P boli založené na Wilcoxonovom teste na porovnanie medzi skupinami pred a po očkovaní. f Rámcové grafy ukázali zmeny pred a po vakcinácii v obsahu monocytov z údajov scRNA-seq (ľavý panel) a klinických laboratórnych meraní (pravý panel). g Rámcové grafy ukázali zmeny v obsahu CD4 + , CD8 + T-buniek, ako aj obsahu lymfocytov (T + B + NK) pred a po vakcinácii z údajov scRNA-seq (ľavé 3 panely) a laboratórnych testov (pravý panel). hDEG identifikované pseudohromadnými vzorkami pred a po vakcinácii. i Analýza nadmerného zastúpenia súborov HALLMARK génov z MSigDB preukazujúca rôzne imunologické vlastnosti pred a po očkovaní.
Použitím grafového zoskupovania aproximácie a projekcie uniformnej rozmanitosti (UMAP) 23 , algoritmu Single-cell Recognition of cell type (SingleR) 24 a manuálnej anotácie založenej na kanonických génových markeroch sme identifikovali 22 bunkových typov alebo podtypov a vykonali diferenciálnu expresnú analýzu medzi všetkými typmi buniek (obr. 3b a doplnková tabuľka S8 ). Bunky (bunkové transkriptómy) zo vzoriek pred (modrá) a po (oranžová) vakcinácia boli zreteľne oddelené v reprezentácii UMAP pre obe kohorty, čo znamenalo, že imunologické vlastnosti sa dosť drasticky zmenili u takmer všetkých zistených typov imunitných buniek a konzistentne u všetkých dobrovoľníkov ( Obr. 3c). Spomedzi 11 párov (pred a po) vzoriek PBMC bolo 10 párov sekvenovaných spolu a jeden pár bol sekvenovaný oddelene v inej dávke. Distribúcie UMAP boli drasticky podobné bez ohľadu na rôzne šarže, čo naznačuje minimálne efekty sekvenčných šarží (doplnkový obrázok S1b ). Dve nezávislé šarže sekvenovania odhalili podobné zmeny pred a po očkovaní, čo naznačuje, že zmeny sú skutočné, zatiaľ čo pri použití metódy korekcie účinku šarže (Harmony 25 ) (doplnkový obrázok S1c–e) by viedlo k nadmernej filtrácii a eliminácii skutočných zmien spôsobených očkovaním. Okrem toho zhlukovanie vzoriek na základe Pearsonovho korelačného koeficientu transkriptómov ukázalo, že vzorky z dvoch kohort (A a B) sa navzájom dobre prelínali pred aj po očkovaní, zatiaľ čo zmeny vyvolané očkovaním bolo možné jasne pozorovať (obr. 3d ). . Preto, aby sme zvýšili štatistickú silu, spojili sme tieto dve kohorty pre následné analýzy.
Na odhalenie rozdielov v zložení bunkového typu pred a po vakcinácii sme vypočítali relatívne percentá všetkých bunkových typov v PBMC každého jedinca na základe údajov scRNA-seq (obr. 3e ). Pozorovali sme zníženie obsahu CD4 + regulačných T buniek (CD4.Treg), CD8 + T buniek (CD8.T) a proliferujúcich CD8 + buniek (CD8.Tprolif) po vakcinácii (obr. 3e ). Zníženie obsahu yδ-T buniek (gd.T.Vd2) bolo tiež významné (obr. 3e ). Na rozdiel od toho očkovanie zvýšilo obsah CD14 + klasických monocytov (Mono.C) (obr. 3e ), čo je v súlade s klinickými laboratórnymi meraniami (obr. 3f). Celkový obsah lymfocytov, ktorý zahŕňal všetky CD4 + T bunky, všetky CD8 + T bunky, B bunky a NK bunky, sa pred a po očkovaní významne nezmenil, čo potvrdili aj klinické laboratórne merania (obr. 3g ). Zhromaždili sme publikovaný súbor údajov od 196 pacientov infikovaných COVID-19 a kontrol 7 a analyzovali sme naše údaje spolu s týmto súborom údajov. Výsledok naznačil, že očkovaním vyvolané zmeny v obsahu buniek všetkých piatich rôznych podtypov imunitných buniek sa tiež zmenili v rovnakých smeroch u pacientov s COVID-19 v porovnaní s kontrolami, s výnimkou proliferujúcich CD8 + T buniek (doplnkový obrázok S2 ).
Na štúdium podrobných zmien génovej expresie vyvolaných očkovaním sme zlúčili jednotlivé vzorky do pseudo-hromadných vzoriek a použili sme test párových vzoriek na identifikáciu rozdielne exprimovaných génov (DEG) (obr. 3h a doplnková tabuľka S9 ). Výrazne upregulované gény sa podieľali na „signalizácii TNFα prostredníctvom NF-κB“, „zápalových reakciách“ a „interakcii cytokín-cytokínový receptor“, „signalizácii IL6-JAK STAT3“, „koagulácii“, „hypoxii“, ktoré boli hlásené pre COVID-19, zatiaľ čo dráhy súvisiace s bunkovým cyklom boli downregulované (obr. 3i ). Tieto výsledky podporili názor, že očkovanie napodobňuje infekciu 6 , 7 , 8 , 9 , 10 , 11,12.
Zmeny génovej expresie špecifické pre subtyp imunitnej bunky odzrkadľovali klinické laboratórne zmeny
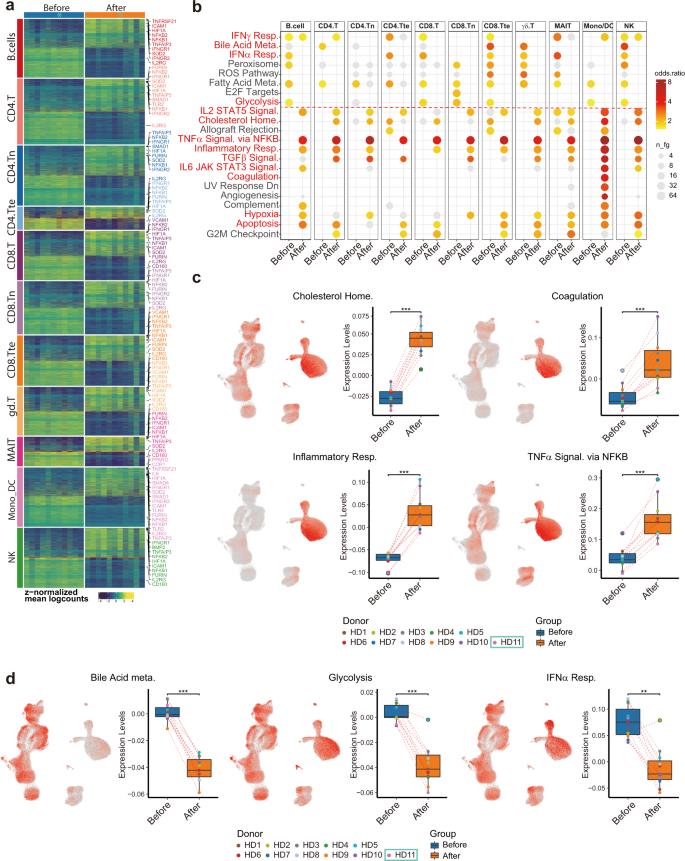
Pred objasnením funkčnej heterogenity a zmien génovej expresie špecifických pre bunkový typ medzi vzorkami pred a po očkovaní sme bunky zoskupili do 11 hlavných typov: (1) CD4 + T bunky v naivnom stave, (2) CD8 v naivnom stave + T bunky, (3) CD4 + pomocné T bunky (vrátane CD4.T, CD4.Treg a CD4.Tprolif), (4) CD8 + cytotoxické T bunky (vrátane CD8.T, CD8B.T a CD8.Tprolif ), (5) MAIT, (6) γδ-T bunky, (7) NK bunky (vrátane NK, NK proliferatívnych), (8) B/plazmablastové bunky (vrátane B buniek a plazmablastov), (9) monocyty/dendritické bunky (vrátane klasických mono, intermediárnych mono, neklasických mono, myeloidných DC1, myeloidných DC2 a plazmacytoidných DC), (10) CD4 + terminálnych efektorových T buniek a (11) CD8+ terminálne efektorové T bunky. Po jedenásť bunka typu kategorizácie, sme vykonali porovnanie vzorky na úrovni agregáciou génovú expresiu cez hlavné typy buniek v rámci každého darcu a potom vykonáva diferenciálnej analýzu expresie pomocou Muscat 26 . Identifikovali sme rozdielne exprimované gény (DEG) medzi všetkými hlavnými bunkovými typmi (obr. 4a a doplnková tabuľka S10 ) a vykonali sme génovú funkčnú analýzu (obr. 4b). Odrážajúc výsledky klinických meraní, gény súvisiace s „homeostázou cholesterolu“, „koaguláciou“ a „zápalovou odpoveďou“ (CXCL8, CD14, IL6 a TNFRSF1B), „signalizácia TNFα prostredníctvom NF-κB“ (NFKB1, NFKB2, NFKBIE, TNFAIP3 a TNFSF9) a „hypoxia“ (HIF1A) boli upregulované. Okrem toho boli upregulované aj gény súvisiace s „signalizáciou TGFp“, „signalizáciou IL2-STAT5“ (IFNGR1, MAPKAPK2 a CASP3) a „signalizáciou IL6-JAK-STAT3“ (obr. 4c ). Aby sme vizualizovali, ktoré typy buniek boli obohatené o tieto podpisy, vykonali sme hodnotenie génového modulu a zobrazili skóre na súradniciach UMAP, ako aj zoskupené krabicové grafy (obr. 4c a doplnková tabuľka S11). Je zaujímavé, že gény „zápalovej odpovede“ boli vysoko exprimované v monocytoch a po očkovaní sa ďalej zvýšili (obr. 4c ), čo naznačuje, že monocyty boli jedným z hlavných typov buniek zúčastňujúcich sa na zápalových reakciách po očkovaní. Na rozdiel od toho boli gény súvisiace s „glykolýzou“, „metabolizmom žlčových kyselín“ a „reakciou na interferón typu I (IFN-α/β) downregulované, čo je v súlade s našimi klinickými údajmi a patofyziológiou COVID-19 13 (obr. 4d ).
A 11 hlavné imunitný bunkovo špecifické Degsy identifikované pseudo-hromadných údajov z kombinácií vzoriek pred a po očkovaní. Boli zahrnuté gény s logFC > 0,5 a úpravou P < 0,05. b Analýza nadmerného zastúpenia HALLMARK génových súborov z MSigDB medzi 11 hlavnými bunkovými typmi preukázala bežné zmeny v génových súboroch reprezentujúcich zmenené imunologické stavy pred a po očkovaní. c , d UMAP vizualizácia zafarbená priemernými expresnými skóre (hladinami) na základe rozdielnej dráhy obohatenia. Rámčekový graf zobrazujúci distribúciu skóre expresie pred a po očkovaní.
Najbežnejšie zmeny vo viacerých podtypoch imunitných buniek odhalili zvýšenie signalizácie NF-κB a zníženie odpovedí IFN-α/β
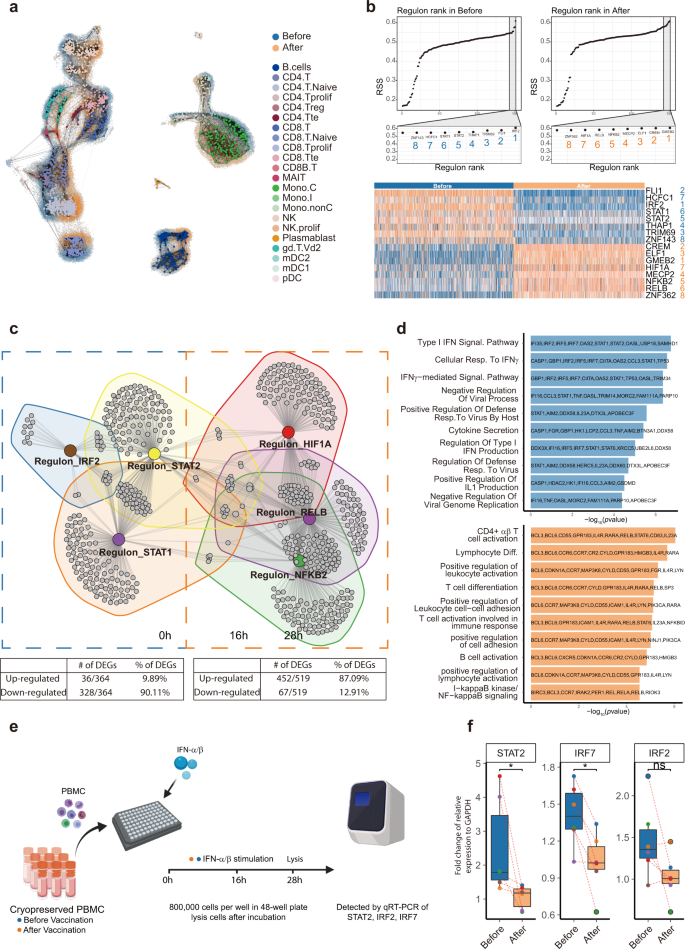
Vzhľadom na to, že zhluky génov dramaticky zmenili svoju expresiu medzi všetkými hlavnými typmi buniek, predpokladali sme, že by mohli existovať niektoré transkripčné faktory slúžiace ako hlavné regulátory vedúce k imunologickým zmenám. Na vyriešenie výpočtových problémov spojených s takým veľkým súborom údajov sme použili algoritmus MetaCell 27 na agregáciu homogénnych skupín buniek do metabuniek a nakoniec sme vytvorili 1 857 metabuniek (893 pred a 964 po očkovaní), ktoré reprezentujú celú štruktúru scRNA-sekv. dáta (obr. 5a ). Tieto metabunky sa potom použili na „odvodzovanie a klastrovanie regulačnej siete jednej bunky (SCENIC)“ 28 , 29vybudovať génové regulačné siete. Pracovný postup vytvoril zoznam 157 „regulónov“, ktoré zahŕňali transkripčné faktory a ich priame ciele. Aktivity regulónu sa hodnotili pomocou AUCell, aby sa získalo priemerné obohatenie všetkých génov patriacich ku každému regulónu v každej metabunke, ako aj priemerné obohatenie génu regulónu vo všetkých 893 metabunkách pred vakcináciou a 964 metabunkách po vakcinácii. Po vakcinácii bolo identifikovaných osem (najaktívnejších) osem regulónov s reguláciou smerom nahor a osem regulónov so zníženou reguláciou (obr. 5b ). Vybrali sme 3 + 3 typické regulóny na vytvorenie regulačnej siete, ako je znázornené na obrázku 5c (doplnková tabuľka S12). Sieť ukázala dve odlišné skupiny, jedna pozostáva z IRF2, STAT1 a STAT2, ktoré boli po očkovaní znížené, a druhá obsahovala RELB, NFKB2 a HIF1A, ktoré boli po očkovaní upregulované. Termíny GO upregulovanej siete súvisia predovšetkým s diferenciáciou lymfocytov, aktiváciou a „tvorbou zárodočného centra“, čo naznačuje, že T bunky a B bunky boli aktivované po očkovaní. Okrem toho bola po očkovaní zvýšená aj signalizácia NF-KB. Downregulovaná sieť bola obohatená o mnohé dráhy súvisiace s interferónmi a sekréciu cytokínov (obr. 5d a doplnková tabuľka S13). To naznačuje, že očkovanie môže inhibovať interferón reakcií v periférnom imunitnom systéme, a to znížením aktivity regulons STAT1, STAT2 a IRF2, ktoré boli považované za master transkripčné faktory, typ I a III interferón signalizácia 30 , 31 .
a Vizualizácia pre metabunky „súvisiace so štruktúrou“ na pôvodných údajoch scRNA-seq. Metabunky boli farebne označené podľa ich anotácií typu buniek. Pôvodné údaje scRNA-seq boli farebne označené „modrou“ a „oranžovou“, aby predstavovali vzorky „pred“ a „po“ očkovaní. b Horné panely: poradie regulónov vo vzorkách pred (vľavo) a po (vpravo) očkovaní na základe skóre regulonovej špecifickosti (RSS). Spodné panely: teplotná mapa najvyšších regulačných aktivít pred (modrá) a po (oranžová) vakcinácia na základe skóre AUCell. Názvy regulónov sú farebne (modrá/oranžová) a číselne kódované (1–8). cSieť regulónov a ich cieľových génov. Nižšie uvedená tabuľka ukazuje podiel génov v rámci regulónov, ktoré boli po očkovaní up- alebo downregulované. d Funkčná anotácia génu a súvisiace gény pred (modrá) a po (oranžová) vakcináciou. e Schematický prehľad experimentu. f Po liečbe IFN-α/β mali PBMC od dobrovoľníkov po očkovaní zníženú expresiu génov spojených s odpoveďami na interferón typu I v porovnaní s tými, ktoré boli pred očkovaním. Použil sa párový Wilcoxonov test. * P < 0,05, n = 6.
Na potvrdenie očkovaním indukovanej inhibície interferónových reakcií odhalených pomocou scRNA-seq sme stimulovali PBMC od očkovaných jedincov pred a 28 dní po očkovaní IFN-a/p. Po 16 hodinách kultivácie a 12 hodinách stimulácie sme použili RT-qPCR na meranie relatívnej expresie hlavných regulátorov IRF2, IRF7 a STAT2. STAT2 a IRF7 boli po vakcinácii významne znížené, avšak IRF2 vykazovali trend zníženia (obr. 5e, f ). Analýzy regulónov ukázali, že stavy periférneho imunitného systému po vakcinácii mali znížené reakcie na interferón typu I, čo svedčí o oslabených všeobecných antivírusových schopnostiach aspoň 28 dní po prvej inokulácii.
Zápalové reakcie v monocytoch vyvolané očkovaním
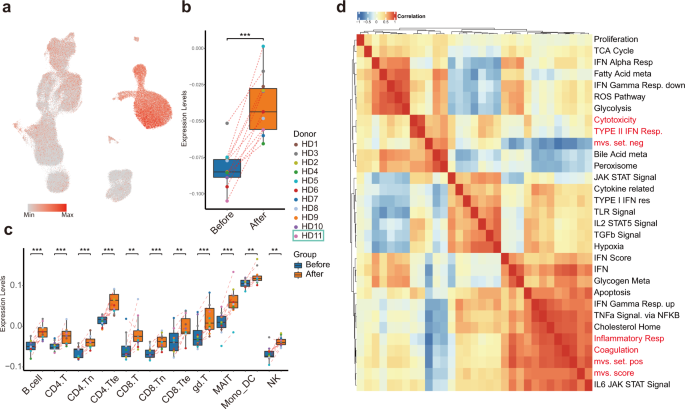
Nedávne správy opísali zachované signatúry imunitnej odpovede hostiteľa na respiračné vírusové infekcie, konkrétne metavírusový podpis (MVS), ktorý je zachovaný aj pri infekcii SARS-CoV-2 32 , 33 . Vyššie skóre MVS je spojené s infekciou 32 , 33 . Celkovo bolo v našom súbore údajov zistených 380 (158 pozitívne a 222 negatívne prispelo k skóre MVS) z 396 (161 pozitívne a 235 negatívne) génov vybraných na meranie MVS. Aby sme preskúmali imunitné reakcie hostiteľa po očkovaní inaktivovaným SARS-CoV-2, oddelili sme pozitívne a negatívne génové sady a vypočítali sme skóre MVS (obr. 6a ). Skóre MVS bolo podstatne vyššie po očkovaní (obr. 6b, c), čo naznačuje, že očkovanie napodobňuje infekciu. Je zaujímavé, že pozitívny súbor génov MVS bol prevažne exprimovaný v monocytoch, zatiaľ čo negatívny súbor v lymfocytoch, čo naznačuje, že po vakcinácii sa vyskytnú rôzne imunitné reakcie špecifické pre bunkový typ (doplnkový obrázok S3a, b ).
UMAP vizualizácia zafarbená MVS skóre. b Skóre MVS v pseudo-hromadných vzorkách kombinujúcich všetky typy buniek ukázali po vakcinácii zvýšenú reguláciu. c Rámcové grafy zobrazujúce distribúciu skóre medzi 11 hlavnými typmi imunitných buniek pred a po očkovaní. d Teplotná mapa korelácie medzi skóre MVS a obohatenými dráhami rozdielne exprimovaných génov pred a po očkovaní.
Aby sme zistili, ktoré dráhy boli spojené s MVS-pozitívnym génovým súborom a MVS-negatívnym génovým súborom, vypočítali sme Spearmanovu koreláciu medzi skóre MVS génových súborov a predtým sme identifikovali rozdielne obohatené dráhy pomocou našich údajov scRNA-seq (obr. 6d ). Najviac korelovaná dráha so skóre MVS a pozitívnym súborom MVS bola „signalizácia zápalovej odpovede“, ktorá bola po vakcinácii výrazne zvýšená v monocytoch spolu s CD14, FPR1, C5AR1, NAMPT, NLRP3, CDKN1A a IFNGR2. Zatiaľ čo MVS-negatívna sada dobre korelovala s „podpisom cytotoxicity“, reprezentovaným expresiou NKG7, CCL4, CST7, PRF1, GZMA, GZMB, IFNG a CCL3, po vakcinácii výrazne klesla v mnohých podtypoch T-buniek, ale nie v NK bunkách (doplnkové Obr. S3c ).
Diskusia
Ide o komplexný výskum patofyziologických zmien, vrátane podrobných imunologických zmien u ľudí po očkovaní proti COVID-19. Výsledky ukázali, že očkovanie okrem stimulácie tvorby neutralizačných protilátok ovplyvňovalo aj rôzne zdravotné ukazovatele vrátane tých, ktoré sa týkali cukrovky, renálnej dysfunkcie, metabolizmu cholesterolu, problémov s koaguláciou, nerovnováhy elektrolytov, a to spôsobom, ako keby dobrovoľníci zažili infekciu. scRNA-seq PBMC od dobrovoľníkov pred a po očkovaní odhalili dramatické zmeny v génovej expresii imunitných buniek, čo nielen odrážalo niektoré klinické laboratórne merania, ale tiež naznačuje zvýšené zápalové reakcie súvisiace s NF-κB, ktoré sa ukázali ako prebiehajúce v klasických monocytoch. Očkovanie tiež zvýšilo klasický obsah monocytov. Okrem toho génový súbor pozitívne prispievajúci k skóre MVS, o ktorom je tiež známe, že je spojený s rozvojom závažných symptómov, bol vysoko exprimovaný v monocytoch. Reakcie interferónu typu I (IFN-a/p), údajne prospešné proti COVID-19, boli po očkovaní znížené. Okrem toho boli negatívne gény MVS vysoko exprimované v lymfocytoch (T, B a NK bunky), avšak po vakcinácii vykazovali zníženú expresiu. Tieto údaje spolu naznačujú, že po očkovaní, aspoň do 28. dňa, okrem vytvorenia neutralizačných protilátok, bol ľudský imunitný systém, vrátane lymfocytov a monocytov, pravdepodobne v zraniteľnejšom stave. údajne prospešné proti COVID-19, boli po očkovaní znížené. Okrem toho boli negatívne gény MVS vysoko exprimované v lymfocytoch (T, B a NK bunky), avšak po vakcinácii vykazovali zníženú expresiu. Tieto údaje spolu naznačujú, že po očkovaní, aspoň do 28. dňa, okrem vytvorenia neutralizačných protilátok, bol ľudský imunitný systém, vrátane lymfocytov a monocytov, pravdepodobne v zraniteľnejšom stave. údajne prospešné proti COVID-19, boli po očkovaní znížené. Okrem toho boli negatívne gény MVS vysoko exprimované v lymfocytoch (T, B a NK bunky), avšak po vakcinácii vykazovali zníženú expresiu. Tieto údaje spolu naznačujú, že po očkovaní, aspoň do 28. dňa, okrem vytvorenia neutralizačných protilátok, bol ľudský imunitný systém, vrátane lymfocytov a monocytov, pravdepodobne v zraniteľnejšom stave.
Je zaujímavé, že naše predbežné údaje ukázali, že ak sme predinkubovali RBD SARS-CoV-2 s PBMC (od dobrovoľníkov pred a po očkovaní) a potom ošetrili bunky IFN-α/β, reakcie na interferón typu I sa v skutočnosti zvýšili. PBMC po očkovaní, čo naznačuje, že možno očkovanie, hoci znížilo všeobecnú antivírusovú schopnosť osoby, zlepšilo adaptívnu imunitnú funkciu špecificky voči SARS-CoV-2 (doplnkový obrázok S4a ). Na druhej strane pri porovnaní PBMC pred očkovaním sa zdá, že predbežná liečba SARS-CoV-2 S-RBD znižuje reakcie interferónu typu I ( P < 0,05, IRF2, IRF7, STAT2) (doplnkový obrázok S4b), čo naznačuje, že prvá expozícia vírusovému peptidu by skutočne spôsobila zníženie reakcií interferónu typu I v PBMC. Tieto údaje in vitro pekne podporili výsledky scRNA-seq.
Stojí za zmienku, že jeden jedinec v kohorte A, ktorý užíval antibiotiká, náhodou nemal zníženú génovú expresiu spojenú s odpoveďami na interferón typu I, a tento jedinec mal tiež najvyšší titer neutralizačných protilátok v rámci kohorty. Ďalej sme vypočítali Pearsonov korelačný koeficient medzi titrami neutralizačných protilátok a zápalovými odpoveďami meranými spriemerovanou génovou expresiou génov spojených so signalizáciou TNFa prostredníctvom NF-KB a odpoveďami interferónu-a (interferón typu I). Výsledky boli 0,32 a 0,39 s P > 0,05 (doplnkový obrázok S4c), čo naznačuje, že zmeny v imunitnej odpovedi a adaptívna imunitná ochrana vakcíny nie sú vo vysokej korelácii. Zostáva určiť, či antibiotiká môžu ovplyvniť účinnosť vakcíny. Je tiež dosť zaujímavé, že kým kohorty A a B mali rôzne profily produkcie protilátok proti SARS-CoV-2, ich výsledky PBMC scRNA-seq boli drasticky podobné, vrátane ich údajov scRNA-seq B-buniek (doplnkový obrázok S5a–c). Treba poznamenať, že po očkovaní by sa väčšina reagujúcich B buniek, najmä tých, ktoré produkujú zrelé protilátky proti COVID-19 (IgG), vrátane pamäťových B buniek, mala primárne nachádzať v periférnych lymfatických tkanivách, ako sú lymfatické uzliny a slezina, zatiaľ čo v obehu by existovalo len niekoľko zrelých B buniek. Preto populácia B-buniek v prípravkoch PBMC nemusí odrážať celé spektrum humorálnej imunity.
Analýzy prezentované v tejto štúdii, najmä scRNA-seq PBMC, sa neuskutočnili pre predchádzajúce hodnotenia vakcín, či už zmeny v génoch súvisiacich s funkciou imunitného systému boli špecifické pre COVID-19 alebo sa dali vo všeobecnosti použiť na iné vakcíny alebo iné typy. očkovacích látok COVID-19 zostáva ešte určiť. Tieto typy podrobných analýz by však mali byť celkovo prospešné pre vývoj a aplikácie vakcín. Naša štúdia predpokladá, že je nevyhnutné zvážiť potenciálny dlhodobý vplyv očkovania na určité zdravotné stavy 34 alebo na celkové ľudské zdravie.
Materiály a metódy
Účastníci, zber klinických údajov a postupy
Do programu boli prijatí zdraví dospelí dobrovoľníci. Všetky subjekty absolvovali fyzikálne vyšetrenie a vyplnili dotazník vyškolenými lekármi. Do štúdie bol zaradený zdravý dospelý vo veku 18–60 rokov s axilárnou teplotou ≤ 37,0 °C, negatívny na test nukleových kyselín SARS-CoV-2 a ochotný dokončiť všetky plánované študijné procesy. Ľudia s epilepsiou, mozgovými alebo duševnými chorobami, alergiami v anamnéze, nekontrolovanými závažnými chronickými ochoreniami a klinicky významnými abnormálnymi biochemickými nálezmi, hematologickými testami boli vylúčení. Vylúčené boli aj tehotné alebo dojčiace ženy. Túto štúdiu schválila Etická komisia Shanghai East Hospital v súlade s princípmi Helsinskej deklarácie (č. 2020 (096)). Pred registráciou boli od všetkých účastníkov získané písomné informované súhlasy.
Celkovo bolo zaradených a očkovaných 11 účastníkov, aby sa vyhodnotila klinická bezpečnosť a dynamické zmeny v imunitnom systéme. Spomedzi nich bolo päť účastníkov (kohorta A) očkovaných dávkou 4 μg inaktivovanej vakcíny SARS-CoV-2 (Vero Cell) v dňoch 1 a 14 a šesť účastníkov (kohorta B) dostalo dávku 4 μg vakcíny v dňoch 1 a 28. Inaktivovaná vakcína SARS-CoV-2 (Vero Cell) (China Biotechnology Group Corporation) bola podaná intramuskulárne do deltového svalu. Všetky vakcíny boli schválené Národným inštitútom pre kontrolu potravín a liečiv v Číne.
Laboratórne testy bezpečnosti vrátane ukazovateľov súvisiacich s infekciou (C-reaktívny proteín, sérový amyloid A proteín), hematologické parametre (počet bielych krviniek, počet neutrofilov, počet lymfocytov, počet monocytov, počet červených krviniek, hemoglobín, počet krvných doštičiek), funkcia koagulácie - súvisiace indexy (protrombínový čas, aktivovaný parciálny tromboplastínový čas/APTT, fibrinogén, protrombínová aktivita/PT, medzinárodný normalizovaný pomer/INR), parametre súvisiace s krvnou glukózou (plazmatická glukóza nalačno, HbA1c), sérové lipidy (celkový cholesterol, triglyceridy, HDL -C, LDL-C), enzýmy súvisiace s funkciou srdca (kreatinínkináza, CK-MB), elektrolyty (draslík, sodík, chlorid, hydrogénuhličitan, celkový vápnik, horčík), biomarkery súvisiace s funkciou pečene (napr. albumín, alanínaminotransferáza /ALT, aspartátaminotransferáza/AST, celkový bilirubín atď.),merali sa markery súvisiace s renálnou funkciou (kreatinín, kyselina močová, dusík v krvi/BUN, odhadovaná rýchlosť glomerulárnej filtrácie/eGFR).
Testovanie protilátok COVID-19 (IgG/IgM).
Množstvo komerčne dostupných súprav na rýchle testovanie protilátok COVID-19 (IgG/IgM) vrátane „Innovita (špecifické pre proteín S)“, „GenBody (špecifické pre proteín N)“, „Livzon (proteíny S + N)“ a „AbKhan ( S + N proteíny)“ sa použili na testovanie anti-COVID-19 (IgM/IgG) pozitivít plazmy dobrovoľníkov pred a v rôznych časoch po očkovaní. Súprava „AbKhan“ bola najcitlivejšia a v tejto štúdii sa použili údaje.
Neutralizačný test protilátok pomocou PRNT
Každá zo vzoriek séra bola testovaná pomocou testu neutralizačného testu redukcie plaku (PRNT) na SARS-CoV-2 (2019-nCoV-WIV04) v laboratóriu BSL-3. Stručne povedané, séra boli tepelne inaktivované pri 56 °C počas 30 minút a zriedené na 1:50, po ktorých nasledovali trojnásobné sériové riedenia (1:50, 1:150, 1:450, 1:1350, 1:4050 a 1: 12 150). Séra boli potom zmiešané so 100 PFU vírusu a inkubované pri 37 ° C počas 1 hodiny. Zmesi na riedenie vírusu a séra a vírusová kontrola sa potom naočkovali do bunkových monovrstiev Vero E6 v 24-jamkových doštičkách počas 1 hodiny pred pridaním prekrývacieho média obsahujúceho 1,5 % metylcelulózu pri 37 °C počas 4 až 5 dní, aby sa umožnil vývoj plakov. Potom boli platne fixované a zafarbené 2% kryštálovou violeťou v 30% metanole počas 30 minút pri teplote miestnosti a plaky boli manuálne spočítané a zmerané.
Príprava jednobunkových suspenzií, príprava jednobunkovej RNA knižnice a sekvenovanie
PBMC boli izolované z heparinizovanej venóznej krvi od zdravých dobrovoľníkov s použitím média Ficoll-Paque TM PLUS (GE Healthcare Inc.) podľa štandardnej centrifugačnej metódy s gradientom hustoty poskytnutej výrobcom. PBMC boli zmrazené v mraziacom médiu (70 % RPMI-1640, 20 % FBS a 10 % DMSO) a skladované v tekutom dusíku až do použitia. Zachytenie jednej bunky a konštrukcia knižnice sa uskutočnili pomocou súpravy Chromium Single Cell 5' Library & Gel Bead kit (10x Genomics) podľa pokynov výrobcu. Knižnice boli sekvenované pomocou platformy Novaseq 6000 (Illumina).
analýza a štatistika údajov scRNA-seq
Údaje o sekvenovaní jednotlivých buniek boli zarovnané a kvantifikované pomocou kallisto/bustools (KB, v0.25.0) 35 proti ľudskému referenčnému genómu GRCh38 stiahnutému z oficiálnej webovej stránky 10x Genomics. Predbežné počty sa potom použili na následné analýzy. Vytvorili sme kanál na spracovanie údajov. Stručne, bunky s menej ako 200 génov boli odfiltrované, logaritmické normalizovaná počíta a horné 3000 vysoko variabilné gény (HVGs) selekcia sa vykonávali Scanpy 36 .
Z HVG sme vylúčili špecifické gény vrátane mitochondriálnych génov, imunoglobulínových génov a génov spojených so slabo podporovanými transkripčnými modelmi (anotované predponou „Rp-“). Potom bola vykonaná Analýza hlavných komponentov (PCA) využitím HVGs a Harmony algoritmus bol použitý na odstránenie dávkové účinky 25 . Použili sme prístup PARC na identifikáciu zhlukov 37 a vybrali sme funkcie pomocou funkcie „FeatureSelectionByEnrichment“ z algoritmu cytograph2 38 , po ktorom nasledovalo ďalšie kolo PCA, Harmony a PARC. Následne sme vypočítali K najbližších susedov v KNN grafe, vykonali sme aproximáciu a projekciu rovnomerného množstva (UMAP) pomocou Pegasuspy 39 a identifikovali sme zhluky pomocou PARC. Okrem toho sme aplikovali Scrublet 40 identifikovať potenciálne dublety.
Kontrola kvality bola aplikovaná na klastre na základe výstupu prvého kola potrubia:
- 1.
Zhluky s viac ako 20 % buniek, z ktorých dubletové skóre > 0,4 boli definované ako zhluky dubletov.
- 2.
Klastre s viac ako 20 % buniek, ktoré mali > 20 % svojich transkriptov mapovaných na mitochondriálne gény, boli definované ako zhluky nízkej kvality.
- 3.
Klastre s viac ako 20 % buniek, ktoré mali < 0, 05 % svojich transkriptov mapovaných na mitochondriálne gény, boli definované ako jadrá.
- 4.
Stredná expresia PPBP, PF4, HBB, HBA2 > 0, čo naznačuje erytrocyty a krvné doštičky.
- 5.
Menej ako 50 buniek.
- 6.
Počet zistených génov < 1000.
- 7.
Pomer priemeru celkových UMI a priemeru detegovaných génov < 2.
- 8.
Scrublet identifikoval dublety.
- 9.
Použitie DBSCAN 41 na odstránenie odľahlých hodnôt.
Po odstránení buniek nízkej kvality sme bunky anotovali pomocou algoritmu jednobunkového rozpoznávania bunkových typov (SingleR) s odkazom na súbory údajov o imunite Monaka 42 .
Kvalifikované bunky sa podrobili následnej analýze. Podobne znova spustíme potrubie na identifikáciu hlavných typov buniek vrátane T buniek (CD3D, CD3E, CD3G, CD40LG, CD8A, CD8B), B buniek (MS4A1, CD79A, CD79B), NK buniek (GNLY, NKG7, TYROBP, NCAM1), a monocyty (CST3, LYZ). Okrem toho sme spustili pipeline na každom type buniek a ďalej identifikovali podtypy na základe SingleR-identifikovaných bunkových typov a dobre charakterizovaných markerov (obr. 3b ).
Porovnanie pomeru imunitných buniek
Pre vzorky z PBMC sme vypočítali proporcie imunitných buniek pre každý hlavný bunkový typ a základné podtypy. Pre každú vzorku sa pomer typu buniek vypočítal počtom buniek v určitom type buniek vydeleným celkovým počtom buniek. Aby sme identifikovali zmeny v proporciách buniek medzi vzorkami v rôznych skupinách, vykonali sme Wilcoxonov test na proporciách jednotlivých hlavných typov buniek, ako aj podtypov buniek v rôznych skupinách (doplnkový obrázok S2 ). Len tie typy buniek so štatisticky významnými rozdielmi ( P < 0,05) v pomeroch sú znázornené na Obr. 3e .
Analýza diferenciálnej expresie, analýza nadmerného zastúpenia génových súborov a moduly podpisu skóre
Aby sme preskúmali zmeny imunologických vlastností, identifikovali sme DEG pomocou muškátového algoritmu 26 s predvolenými parametrami. V stručnosti, najprv sme zhrnuli údaje, zhrnuli sme UMI naprieč bunkami pre každého zdravého darcu, aby sme vytvorili hromadný profil UMI v štýle RNA-seq pre každú vzorku. Potom sa agregované počty načítali do funkcie pbDS na identifikáciu stupňov a tepelné mapy sa vykresľovali pomocou funkcie pbHeatmap. Analýza nadmerného zastúpenia génovej sady DEGs (logFC > 0,5 a upravené P < 0,05) sa uskutočnila pomocou jednostranného Fisherovho presného testu (ako je implementovaný v balíku „gsfisher“ R) s génmi „HALLMARK“, „KEGG“ a „REACTOME“. sady odvodené od MSigDB. Génové sady s P < 0,05 sa považovali za významné. Skóre modulu podpisu sa vypočítalo pomocou funkcie „AddModuleScore“ s predvolenými nastaveniami v Seurat. V stručnosti, pre každú bunku, skóre bol definovaný ako priemerný expresie podpisový génu odpočítaním priemerného expresiu zoznamu zodpovedajúcich kontrolného génu 43 . Zoznamy génov použité na analýzu sú uvedené v doplnkovej tabuľke S11 .
Metacell analýza
Na analýzu údajov sme použili balík R „MetaCell“ 27 . Odstránili sme špecifické mitochondriálne gény, imunoglobulínové gény a gény spojené so slabo podporovanými transkripčnými modelmi (anotované predponou „Rp-“). Potom sme filtrovali bunky s menej ako 500 UMI. Génové vlastnosti boli vybrané pomocou parametra Tvm = 0,08 a minimálneho celkového počtu UMI > 100. Následne sme vykonali hierarchické zhlukovanie korelačnej matice medzi týmito génmi (filtrovanie génov s nízkym pokrytím a výpočtovú koreláciu pomocou down-sampled matice UMI) a vybrali sme génové zhluky obsahujúce kotviace gény. Použili sme K = 100 a 500 iterácií bootstrapu a inak štandardné parametre. Metabunky boli označené najhojnejšími typmi buniek tvoriacich každú metabunku.
Analýza génovej regulačnej siete
Na identifikáciu a hodnotenie aktivity regulónu sme použili pySCENIC 28 , 29pracovný tok na log-normalizovaných údajoch metabuniek na určenie súborov koexprimovaných génov. Spojili sme priame ciele s ich zodpovedajúcimi transkripčnými faktormi pomocou databáz RcisTarget (v1.2.1) a zachovali sme predpokladané downstream gény s obohatenými motívmi DNA na 10 kb alebo 500 bp od miesta začiatku transkripcie (normalizované skóre obohatenia > 3). Nakoniec sme použili funkciu AUCell na hodnotenie aktivity každého regulónu naprieč bunkami v súbore údajov, ktorý sa vypočítal ako súčet génov vyjadrených na regulón a vytvorili matice binárnej aktivity na základe medzných hodnôt manuálne upravených po kontrole distribúcie skóre AUC. Skóre regulonovej špecifickosti (RSS) sa vypočítali pomocou funkcie „regulon_specificity_scores“ z algoritmu pySCENIC s predvolenými parametrami.
Analýza IFN-a/p odozvy PBMC
PBMC boli izolované z heparinizovanej krvi pomocou Ficoll-Hypaque pri 400 x g počas 30 minút. PBMC (1 x 10 6 ml -1 ) darcov pred a po vakcinácii boli potom nasadené na 48-jamkové kultivačné doštičky s RPMI-1640 s obsahom 5% knockout sérového výmenu a 0,032% heparín. Nasledujúci deň sa médium vymenilo a bunky sa ošetrili 100 ng/ml IFN-a a 10 ng/ml IFN-p počas 12 hodín. Niektoré bunky boli vopred ošetrené 250 ng/ml RBD počas 16 hodín, po čom nasledovalo ošetrenie IFN-a/p počas 12 hodín. Po premytí a extrakcii celkovej RNA sa uskutočnila kvantitatívna PCR v reálnom čase na detekciu expresie génov spojených s reakciou na interferón typu I. Zmeny násobku vzhľadom na GAPDH boli vypočítané pomocou 2- AACta vyjadrené ako priemer ± SEM. Rozdiely medzi skupinami sa hodnotili pomocou párového Studentovho t- testu a považovali sa za významné, keď P < 0,05.
Štatistická analýza
Klinické údaje boli zhrnuté pomocou priemeru (štandardná odchýlka), mediánu (Q1, Q3) alebo čísla (v percentách), ak to bolo vhodné. Wilcoxonov test so znamienkom sa použil na porovnanie párových mediánov v priebehu času pre laboratórne charakteristiky. Okrem toho sa použil Wilcoxon sum-rank test na porovnanie mediánových zmien oproti východiskovej hodnote medzi kohortami A a B. Nežiaduce udalosti sme ohodnotili podľa stupnice vydanej Čínskou národnou správou medicínskych produktov ( https://www.nmpa.gov. cn/xxgk/ggtg/qtggtg/20191231111901460.html ) a posúdenie výsledkov laboratórnych testov bolo založené na rozmedzí referenčných hodnôt miestnej populácie. Všetky štatistické testy boli obojstranné. Štatistická významnosť bola definovaná ako P ≤ 0,05. Štatistické analýzy sa uskutočnili s použitím SAS v9.4 (SAS Institute Inc., Cary, NC, USA).
Prístupové čísla pre sekvenčné nespracované údaje a spracované údaje v tomto dokumente sú archív sekvencií genómu v BIG Data Center (GSA, Pekinský inštitút genomiky, Čínska akadémia vied): HRA001150.
Referencie
- 1.
Mulligan, MJ a kol. Štúdia fázy I/II RNA vakcíny COVID-19 BNT162b1 u dospelých. Nature 586 , 589-593 (2020).
- 2.
Jackson, LA a kol. mRNA vakcína proti SARS-CoV-2 – predbežná správa. N. Engl. J. Med. 383 , 1920–1931 (2020).
- 3.
Xia, S. a kol. Bezpečnosť a imunogenicita inaktivovanej vakcíny SARS-CoV-2, BBIBP-CorV: randomizovaná, dvojito zaslepená, placebom kontrolovaná štúdia fázy 1/2. Lancet Infect. Dis. 21 , 39-51 (2021).
- 4.
Ramasamy, MN a kol. Bezpečnosť a imunogenicita vakcíny ChAdOx1 nCoV-19 podávanej v režime prime-boost u mladých a starých dospelých (COV002): jednoducho zaslepená, randomizovaná, kontrolovaná štúdia fázy 2/3. Lancet 396 , 1979 – 1993 (2020).
- 5.
Xia, S. a kol. Účinok inaktivovanej vakcíny proti SARS-CoV-2 na výsledky bezpečnosti a imunogenicity: predbežná analýza 2 randomizovaných klinických štúdií. J. Am. Med. Doc. 324 , 951-960 (2020).
- 6.
Meckiff, BJ a kol. Nerovnováha regulačných a cytotoxických SARS-CoV-2-reaktívnych CD4(+) T buniek v COVID-19. Cell 183 , 1340-1353.e16 (2020).
- 7.
Ren, X. a kol. Imunitné vlastnosti COVID-19 odhalené rozsiahlym jednobunkovým transkriptómovým atlasom. Bunka https://doi.org/10.1016/j.cell.2021.01.053 (2021).
- 8.
Bernardes, JP a kol. Pozdĺžne multi-omické analýzy identifikujú reakcie megakaryocytov, erytroidných buniek a plazmablastov ako charakteristické znaky závažného ochorenia COVID-19. Imunita 53 , 1296–1314.e99 (2020).
- 9.
Su, Y. a kol. Multi-Omics rieši prudký posun chorobného stavu medzi miernym a stredne závažným ochorením COVID-19. Cell 183 , 1479-1495.e20 (2020).
- 10.
Wen, W. a kol. Imunitný bunkový profil pacientov s COVID-19 v štádiu zotavenia pomocou jednobunkového sekvenovania. Cell Discov. 6 , 31 (2020).
- 11.
Heming, M. a kol. Neurologické prejavy COVID-19 sa vyznačujú vyčerpaním T buniek a dediferencovanými monocytmi v cerebrospinálnej tekutine. Imunita 54 , 164–175.e6 (2021).
- 12.
Flament, H. a kol. Výsledok infekcie SARS-CoV-2 je spojený s aktiváciou buniek MAIT a cytotoxicitou. Nat. Immunol. 22 , 322-335 (2021).
- 13.
Hadjadj, J. a kol. Zhoršená aktivita interferónu typu I a zápalové reakcie u ťažkých pacientov s COVID-19. Science 369 , 718-724 (2020).
- 14.
Kusnadi, A. a kol. Ťažko chorí pacienti s COVID-19 vykazujú zhoršené znaky vyčerpania v CD8(+) T bunkách reaktívnych na SARS-CoV-2. Sci. Immunol . 6 , https://doi.org/10.1126/sciimmunol.abe4782 (2021).
- 15.
Carissimo, G. a kol. Imunofenotypizácia plnej krvi odhaľuje pomer nezrelých neutrofilov a T-buniek VD2 ako skorý marker závažného ochorenia COVID-19. Nat. komun. 11 , 5243 (2020).
- 16.
Guan, WJ a kol. Klinické charakteristiky koronavírusovej choroby 2019 v Číne. N. Engl. J. Med. 382 , 1708 – 1720 (2020).
- 17.
Huang, C. a kol. Klinické znaky pacientov infikovaných novým koronavírusom z roku 2019 vo Wu-chane v Číne. Lancet 395 , 497-506 (2020).
- 18.
Lau, EHY a kol. Titre neutralizačných protilátok pri infekciách SARS-CoV-2. Nat. Spoločné. 12 , 63 (2021).
- 19.
Lim, S., Bae, JH, Kwon, HS & Nauck, MA COVID-19 a diabetes mellitus: od patofyziológie ku klinickému manažmentu. Nat. Endocrinol. 17 , 11 – 30 (2021).
- 20.
Codo, AC a kol. Zvýšené hladiny glukózy podporujú infekciu SARS-CoV-2 a odpoveď monocytov prostredníctvom osi závislej od HIF-1alfa/glykolýzy. Cell Metab. 32 , 437-446.e5 (2020).
- 21.
Lippi, G., South, AM & Henry, BM Nerovnováha elektrolytov u pacientov s ťažkým koronavírusovým ochorením 2019 (COVID-19). Ann. Clin. Biochem. 57 , 262-265 (2020).
- 22.
Zhang, Y. a kol. Koagulopatia a antifosfolipidové protilátky u pacientov s Covid-19. N. Engl. J. Med. 382 , e38 (2020).
- 23.
Becht, E. a kol. Zníženie rozmerov pre vizualizáciu údajov jednej bunky pomocou UMAP. Nat. Biotechnol . https://doi.org/10.1038/nbt.4314 (2018).
- 24.
Aran, D. a kol. Referenčná analýza pľúcneho jednobunkového sekvenovania odhaľuje prechodný profibrotický makrofág. Nat. Immunol. 20 , 163 – 172 (2019).
- 25.
Korsunsky, I. a kol. Rýchla, citlivá a presná integrácia jednobunkových dát s Harmony. Nat. Methods 16 , 1289-1296 (2019).
- 26.
Crowell, HL a kol. muscat deteguje prechody stavu špecifické pre subpopuláciu z údajov transkriptomiky jednej bunky s viacerými vzorkami. Nat. komun. 11 , 6077 (2020).
- 27.
Baran, Y. a kol. MetaCell: analýza dát jednobunkovej RNA-seq pomocou K-nn grafových oblastí. Genome Biol. 20 , 206 (2019).
- 28.
Van de Sande, B. a kol. Škálovateľný pracovný postup SCENIC pre analýzu regulačnej siete génov s jednou bunkou. Nat. Protoc. 15 , 2247-2276 (2020).29.
Aibar, S. a kol. SCENIC: jednobunková regulačná sieťová inferencia a klastrovanie. Nat. Methods 14 , 1083-1086 (2017).
- 30.
Mu, J. a kol. Proteín SARS-CoV-2 N antagonizuje signalizáciu interferónu typu I potlačením fosforylácie a jadrovej translokácie STAT1 a STAT2. Cell Discov. 6 , 65 (2020).
- 31.
Boudewijns, R. a kol. Signalizácia STAT2 obmedzuje šírenie vírusu, ale vedie k ťažkému zápalu pľúc u škrečkov infikovaných SARS-CoV-2. Nat. komun. 11 , 5838 (2020).32.
Andres-Terre, M. a kol. Integrovaná multikohortová analýza identifikuje zachované transkripčné podpisy naprieč viacerými respiračnými vírusmi. Imunita 43 , 1199-1211 (2015).
- 33.
Zheng, H. a kol. Multikohortová analýza imunitnej odpovede hostiteľa identifikuje konzervované ochranné a škodlivé moduly spojené so závažnosťou medzi vírusmi. Imunita , https://doi.org/10.1016/j.immuni.2021.03.002 (2021).
- 34.
Hviid, A., Hansen, JV, Frisch, M. & Melbye, M. Očkovanie proti osýpkam, mumpsu, ružienke a autizmu. Ann. Stážista. Med. 171 , 388 (2019).
- 35.
Bray, NL, Pimentel, H., Melsted, P. & Pachter, L. Takmer optimálna pravdepodobnostná kvantifikácia RNA-sekv. Nat. Biotechnol. 34 , 525-527 (2016).
- 36.
Wolf, FA, Angerer, P. & Theis, FJ SCANPY: rozsiahla analýza dát jednobunkovej génovej expresie. Genome Biol. 19 , 15 (2018).
- 37.
Stassen, SV a kol. PARC: ultrarýchle a presné zoskupovanie fenotypových údajov miliónov jednotlivých buniek. Bioinformatics 36 , 2778-2786 (2020).
- 38.
Zeisel, A. a kol. Molekulárna architektúra nervového systému myši. Cell 174 , 999-1014.e22 (2018).
- 39.
Li, B. a kol. Cumulus poskytuje cloudovú analýzu údajov pre rozsiahlu jednobunkovú a jednojadrovú RNA-seq. Nat. Methods 17 , 793-798 (2020).
- 40.
Wolock, SL, Lopez, R. & Klein, AM Scrublet: výpočtová identifikácia bunkových dubletov v jednobunkových transkriptomických dátach. Cell Syst. 8 , 281-291.e9 (2019).
- 41.
Ester, M., Kriegel, H.-P., Sander, J. & Xu, X. Algoritmus založený na hustote na objavovanie zhlukov vo veľkých priestorových databázach so šumom. Kdd 96 , 226-231 (1996).
- 42.
Monaco, G. a kol. Signatúry RNA-Seq normalizované množstvom mRNA umožňujú absolútnu dekonvolúciu typov ľudských imunitných buniek. Cell Rep 26 , 1627-1640.e27 (2019).
- 43.
Tirosh, I. a kol. Rozoberanie mnohobunkového ekosystému metastatického melanómu jednobunkovou RNA-sekv. Science 352 , 189 – 196 (2016).
Poďakovanie
Ďakujeme pánovi Orionovi S. Fanovi z UC Davis za úpravu rukopisu. Táto práca bola financovaná z národného kľúčového programu výskumu a vývoja (2020YFC2002800); Špičkové disciplíny (typ IV) inštitúcií vyššieho vzdelávania v Šanghaji; Hlavný program rozvojového fondu pre národnú demonštračnú zónu inovácií Zhangjiang v Šanghaji < Strategická biobanka kmeňových buniek a platforma transformácie klinickej technológie kmeňových buniek > (ZJ2018-ZD-004); Projekt Pudong New Area Klinická tradičná čínska medicína najvyššej disciplíny (PDZY-2018-0603), ako aj projekt BE2020026 kľúčového programu výskumu a vývoja Jiangsu.
5.12.2021 v spolupráci s report24
Položili ste si niekedy otázku, prečo je stále viac ľudí chorých, hoci medicína a ochrana životného prostredia stále tvrdia, že je lepšie a lepšie?
Zamysleli ste sa niekedy nad tým, prečo sú voľby zbytočné?
Premýšľali ste niekedy nad tým, prečo je všetko otočené hore nohami?
V jednej knihe a celkom zaujímavej „Prebudenie začína“ sa drzým a srdečným hlasom rozpráva o všetkom, čo ste vždy chceli vedieť, ale nikdy ste sa neodvážili opýtať.
Táto práca stavia most k traume, do ktorej sme nútení a z ktorej sa môžeme oslobodiť až po prebudení.
Spracoval: ® OZ Dôstojnosť Slovensko v spolupráci s novinármi v zahraničí. Všetky práva vyhradené!!
Potrebujeme vašu pomoc: Bez vašej pomoci by sme toto nedokázali.
Neziskový sektor: SLSP
Názov účtu: Dôstojnosť Slovenska
SK28 0900 0000 0051 7971 8989
Všetky práva vyhradené OZ Dôstojnosť Slovenska. Zdieľanie dovolené.